题目内容
11、在如图的装置中,用弹簧夹夹紧a处的橡皮管,以锌粒和稀硫酸为原料,可制取氢气.某次实验后锥形瓶中锌粒已耗尽,稀硫酸仍有剩余,液面上方充满了氢气.若想赶出这些氢气进行收集利用,可打开a处的弹簧夹,从a处往锥形瓶中通入一定量的( )
0

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
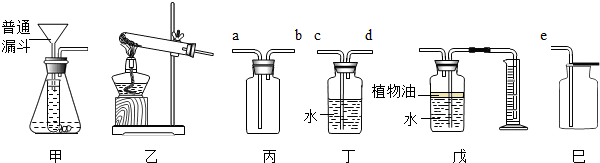
小钱和小鸣同学在实验室里进行的一些化学探究实验,下图是他们进行实验的一些装置图.
(1)他们利用图1装置探究质量守恒定律的实验,实验过程如下表.
①实验中盐酸与大理石反应后出现橡皮塞被弹出来的情况,其可能的原因是 .
②小钱同学认为实验过程中缺少一个重要步骤,这个步骤是 .
③实验时 (选填“可以”或“不可以”)用硫酸代替盐酸,原因是 .
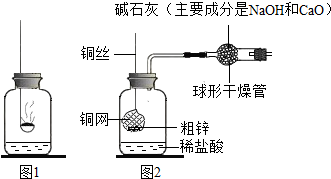
(2)他们还制作了一套如图2的装置,并用该装置测定粗锌样品的含锌量.
①称量10.0g粗锌放在铜网中,按图将仪器组装好以后,称得仪器和药品总质量为120.0g.②将铜网插人足量稀盐酸中,充分反应,可以观察到的实验现象为 ,反应的化学方程式 .
③反应完全后,称得装置总质量为119.8g.则粗锌的纯度为 .
④该实验中碱石灰的作用是 .若不用碱石灰,则所测定的粗锌纯度 (填“偏大”、“偏小”或“无影响”.不考虑空气中C02和H2O对实验的影响).
⑤若将粗锌换成石灰石,原实验方案 (填“能”或“不能”)用于石灰石样品纯度的测定,理由是 .

(1)他们利用图1装置探究质量守恒定律的实验,实验过程如下表.
| 实验过程 | 实验数据记录 |
| 在瓶底放入少量盐酸,将少量大理石粉末放在燃烧匙上,塞紧橡皮塞. | 应记录的实验数据是 |
| 将燃烧匙上的大理石粉末抖下,使其与盐酸接触. | 应记录的实验数据是 |
②小钱同学认为实验过程中缺少一个重要步骤,这个步骤是
③实验时
(2)他们还制作了一套如图2的装置,并用该装置测定粗锌样品的含锌量.
①称量10.0g粗锌放在铜网中,按图将仪器组装好以后,称得仪器和药品总质量为120.0g.②将铜网插人足量稀盐酸中,充分反应,可以观察到的实验现象为
③反应完全后,称得装置总质量为119.8g.则粗锌的纯度为
④该实验中碱石灰的作用是
⑤若将粗锌换成石灰石,原实验方案

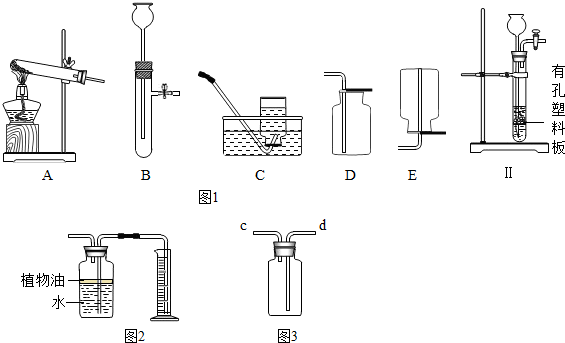
 为测定空气中氧气的含量,小华同学打算设计如下方案:选用实际容积为50mL的具支试管作反应容器,将过量的铜粉放入试管,用橡皮塞塞紧具支试管,通过导管与实际容积为60mL且润滑性很好的针筒注射器组成如图的实验装置.请回答下列问题:
为测定空气中氧气的含量,小华同学打算设计如下方案:选用实际容积为50mL的具支试管作反应容器,将过量的铜粉放入试管,用橡皮塞塞紧具支试管,通过导管与实际容积为60mL且润滑性很好的针筒注射器组成如图的实验装置.请回答下列问题: