题目内容
5.已知常温下氢氧化钙的溶解度为0.165g,常温下的饱和溶液石灰水中溶质的质量分数为0.165%,100g常温下的饱和石灰水可吸收二氧化碳气体0.098g,而常温下很容易配制8%的氢氧化钠溶液,100g 8%的氢氧化钠溶液可吸收二氧化碳气体4.4g,因此化学实验中检验二氧化碳气体用饱和石灰水,而吸收二氧化碳气体常用氢氧化钠溶液.分析 根据溶质质量分数等于溶质质量和溶液质量的比值,氢氧化钙和二氧化碳反应生成碳酸钙沉淀和水,氢氧化钠和二氧化碳反应会生成碳酸钠和水进行分析.
解答 解:饱和溶液石灰水中溶质的质量分数为:$\frac{0.165g}{100.165g}$×100%=0.165%,
100g常温下的饱和石灰水可吸收二氧化碳气体为x
Ca(OH)2+CO2=CaCO3↓+H2O
74 44
100g×0.165% x
$\frac{74}{100g×0.165%}$=$\frac{44}{x}$
x=0.098g
设100g 8%的氢氧化钠溶液可吸收二氧化碳气体为y
2NaOH+CO2=Na2CO3+H2O
80 44
100g×8% y
$\frac{80}{100g×8%}$=$\frac{44}{y}$
y=4.4g
所以化学实验中检验二氧化碳气体用饱和石灰水,吸收二氧化碳气体常用氢氧化钠溶液.
故答案为:0.165%,0.098g,4.4g,饱和石灰水,氢氧化钠溶液.
点评 本题主要考查了氢氧化钠和氢氧化钠的性质和溶解度,难度不大,需要在平时的学习中加强记忆.

练习册系列答案
 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案
相关题目
15.木糖醇(C5H12O5)是一种广泛用于口香糖的物质.下列有关木糖醇的说法正确的是( )
| A. | 木糖醇的相对分子质量为152g | |
| B. | 木糖醇中碳、氢、氧元素的质量比是5:12:5 | |
| C. | 木糖醇中碳、氢、氧原子的个数比是15:3:20 | |
| D. | 该物质中碳元素的质量分数为:$\frac{12×5}{12×5+1×12+16×5}$×100%≈39.5% |
16.一定条件下,在一个密闭器内发生某反应,测得反应前后各物质的质量如表所示,下列说法正确的是( )
| 物质 | CO2 | O2 | H2O | W |
| 反应前质量(g) | 6 | 58 | 5 | 23 |
| 反应后质量(g) | X | 10 | 32 | 0 |
| A. | 该反应属于化合反应 | |
| B. | W是一种由碳、氢两种元素组成的化合物 | |
| C. | X的值为44 | |
| D. | W是一种由碳、氢、氧三种元素组成的化合物 |
10.下列说法不正确的是的( )
| A. | 公共场所“禁烟”是不合理的 | |
| B. | 香烟的烟气中含有很多有毒物质,其中就有CO | |
| C. | 香烟中的焦油对人体是没有危害的 | |
| D. | 长期吸烟的人,易患冠心病、肺气肿和肺癌等. |
15.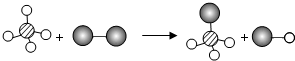 下图表示两种物质发生的化学反应,其中相同的球代表同种原子,小球间的短线代表原子间的结合,下列说法正确的是( )
下图表示两种物质发生的化学反应,其中相同的球代表同种原子,小球间的短线代表原子间的结合,下列说法正确的是( )
 下图表示两种物质发生的化学反应,其中相同的球代表同种原子,小球间的短线代表原子间的结合,下列说法正确的是( )
下图表示两种物质发生的化学反应,其中相同的球代表同种原子,小球间的短线代表原子间的结合,下列说法正确的是( )| A. | 图示中只有三种分子 | B. | 图示中没有单质 | ||
| C. | 该反应中反应物分子个数比为1:1 | D. | 该反应中分子、原子种类都不变 |
 某兴趣小组根据实验室提供的仪器和药品进行了氧气的制备实验.某兴趣小组根据实验室提供的仪器和药品进行了氧气的制备实验.
某兴趣小组根据实验室提供的仪器和药品进行了氧气的制备实验.某兴趣小组根据实验室提供的仪器和药品进行了氧气的制备实验.