题目内容
8.食盐水中含有杂质CaCl2和MgSO4,依次加入过量Ba(OH)2(填化学式,下同)和Na2CO3溶液后过滤,向滤液中加入过量盐酸后,将溶液蒸发;蒸发所用的仪器有酒精灯、玻璃棒、铁架台和蒸发皿.[提示:Mg(OH)2、BaSO4、BaCO3难溶于水].分析 食盐水中少量MgSO4和CaCl2杂质都溶于水,要想将杂质除去必须将MgSO4和CaCl2杂质转化为沉淀;要先加过量的Ba(OH)2溶液除去硫酸根离子和镁离子,然后用Na2CO3溶液去除过量的钡离子和钙离子;注意Na2CO3溶液要在Ba(OH)2溶之后加入,要先除硫酸根离子和镁离子,然后再除钙离子,碳酸钠溶液可以除去过量的钡离子,如果加反了,过量的钡离子无法除去;盐酸要放在最后,来除去过量的Ba(OH)2和Na2CO3
溶液.
解答 解:食盐水中少量MgSO4和CaCl2杂质都溶于水,要想将杂质除去必须将MgSO4和CaCl2杂质转化为沉淀;可采取加水溶解→加入过量Ba(OH)2溶液,与MgSO4发生反应,生成BaSO4沉淀和氢氧化镁沉淀→加过量Na2CO3溶液,与CaCl2和①中过量Ba(OH)2溶液发生反应,生成CaCO3沉淀和BaCO3沉淀和氯化钠→过滤,滤出上述步骤生成的沉淀→加适量盐酸,与过量Na2CO3溶液发生反应,生成氯化钠、水和二氧化碳气体→加热蒸发得到晶体.蒸发所用的仪器有酒精灯、玻璃棒、铁架台和蒸发皿.
故答案为:Ba(OH)2 盐酸 蒸发皿
点评 物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(反应后不能引入新的杂质)是正确解题的关键.

练习册系列答案
相关题目
12.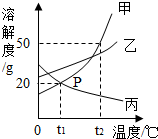 甲、乙、丙三种不含结晶水的固体物质的溶解度曲线如图所示,下列说法中正确的是( )
甲、乙、丙三种不含结晶水的固体物质的溶解度曲线如图所示,下列说法中正确的是( )
 甲、乙、丙三种不含结晶水的固体物质的溶解度曲线如图所示,下列说法中正确的是( )
甲、乙、丙三种不含结晶水的固体物质的溶解度曲线如图所示,下列说法中正确的是( )| A. | t2℃时将50g甲物质放入50g水中,所得溶液中溶质的质量分数为50% | |
| B. | t1℃时三种物质的溶解度大小关系甲>乙>丙 | |
| C. | 将等质量的甲、乙、丙三种配制成t2℃时的饱和溶液,需要水的质量:甲>乙>丙 | |
| D. | 当甲物质中混有少量的丙物质可采取降温结晶的方法提纯甲 |
19.水是我们日常生活必不可少的物质,下列有关水的说法正确的是( )
| A. | 活性炭吸附水中的色素和异味是化学变化 | |
| B. | 用过滤的方法可以使硬水软化 | |
| C. | 可用肥皂水区分硬水与软水 | |
| D. | 水通电分解产生氢气和氧气质量比为2:1 |
16.下列知识整理的内容有错误的一组是( )
| A | 从分子的角度认识 | B | 实验操作的注意事项 |
| 花香四溢--分子不断运动; 水结成冰--分子间隔改变; 水的电解--分子发生改变; | 制取气体--先检查装置的气密性; 加热试管--先预热; 点燃可燃性气体--先验纯; | ||
| C | 物质的分类 | D | 除杂的方法 |
| 有多种物质组成--混合物; 由一种分子构成--纯净物; 含有氧元素的化合物--氧化物; | 铜粉中混有铁粉--用磁铁吸引; 氢气中混有水蒸气--通过浓硫酸; 氯化钠中混有碳酸钙--溶解、过滤、蒸发; |
| A. | A | B. | B | C. | C | D. | D |
3.保护环境人人有责.下列不利于改善环境的做法是( )
| A. | 随意丢弃废旧电池 | B. | 禁止工业污水任意排放 | ||
| C. | 严禁公共场所吸烟 | D. | 治理建筑工地扬尘污染 |
13.近年来我国多地出现雾霾天气,下列各项与形成雾霾无关的是( )
| A. | 太阳能发电 | B. | 汽车尾气 | C. | 煤炭燃烧 | D. | 建筑工地扬尘 |
20.鉴别氢氧化钠溶液和氢氧化钙溶液,应选用的试剂是( )
| A. | 通入CO2气体 | B. | 稀盐酸 | C. | 紫色石蕊试液 | D. | 无色酚酞试液 |
17.化学源于生活,生活中的下列做法不正确的是( )
| A. | 霉变花生清洗后直接食用 | |
| B. | 液化气泄漏时关闭阀门并开窗通风 | |
| C. | 用灼烧的方法鉴别羊毛纤维和涤纶纤维 | |
| D. | 食用适量富含维生素A的动物肝脏可预防夜盲症 |