题目内容
海水中含有少量的氯化镁,海边盛产贝壳(主要成分是CaCO3).以海水和贝壳为原料生产镁的大致程序是:
电解熔融的无水Mg Cl2得到金属镁和氯气(Cl2)
步骤①中需完成的分解反应是:________;
化合反应是:________;
步骤①和②中发生的两个复分解反应是:________,
________.
由无水Mg Cl2得到金属镁的化学方程式为:________.
答案:
解析:
解析:
|
解答:步骤①中需完成的: 分解反应是:CaCO3 化合反应是:CaO+H2O 步骤①和②中发生的两个复分解反应分别是: Mg Cl2+Ca(OH)2 Mg(OH)2+2HCl 电解熔融的无水Mg Cl2的化学方程式为: Mg Cl2 |

练习册系列答案
相关题目
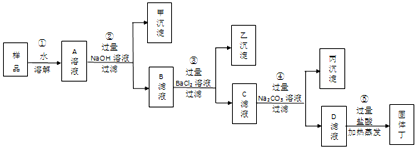
| 通过海水晒盐的方法得到的仅仅是粗盐,其中还含有少量的硫酸钠、氯化镁、氯化钙等杂质,它们在溶液中主要以SO42-、Ca2+、Mg2+的形式存在.为将这些杂质除净,可向食盐溶液分别加过量的氢氧化钠、碳酸钠、氯化钡溶液,然后加入盐酸调至溶液pH=7,最后经过滤、蒸发得到精盐. 一些物质的溶解性表(室温)
|
| A、Na2CO3、BaCl2、NaOH、过滤、HCl |
| B、NaOH、BaCl2、Na2CO3、过滤、HCl? |
| C、BaCl2、Na2CO3、NaOH、过滤、HCl |
| D、BaCl2、NaOH、Na2CO3、过滤、HCl |
通过海水晒盐的方法得到的仅仅是粗盐,其中还含有少量的硫酸钠、氯化镁、氯化钙等杂质,它们在溶液中主要以SO42-、Ca2+、Mg2+的形式存在.为将这些杂质除净,可向食盐溶液分别加过量的氢氧化钠、碳酸钠、氯化钡溶液,然后加入盐酸调至溶液pH=7,最后经过滤、蒸发得到精盐.
一些物质的溶解性表(室温)
| OH- | Cl- | SO42- | CO32- | |
| Na+ | 溶 | 溶 | 溶 | 溶 |
| Ca2+ | 微 | 溶 | 微 | 不 |
| Mg2+ | 不 | 溶 | 溶 | 微 |
| Ba2+ | 溶 | 溶 | 不 | 不 |
- A.Na2CO3、BaCl2、NaOH、过滤、HCl
- B.NaOH、BaCl2、Na2CO3、过滤、HCl?
- C.BaCl2、Na2CO3、NaOH、过滤、HCl
- D.BaCl2、NaOH、Na2CO3、过滤、HCl