题目内容
11. 某同学利用如图所示的装置测定空气中氧气的含量(体积分数).请根据他的操作回答下列问题:
某同学利用如图所示的装置测定空气中氧气的含量(体积分数).请根据他的操作回答下列问题:(1)检查整个装置的气密性后,将c处的止水夹夹紧,点燃红磷后,迅速插入左边的广口瓶中;红磷燃烧时最明显的现象是产生大量白烟;红磷燃烧的文字表达式(或符号表达式)为磷+氧气$\stackrel{点燃}{→}$五氧化二磷(4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5).
(2)待燃烧停止,将c处的止水夹打开.结果发现烧杯中的水进入到广口瓶中,且占广口瓶体积的约$\frac{1}{8}$,则该同学测得的空气中氧气的体积分数为12.5%.与理论值21%相比较,产生误差的原因很可能是②③.(填序号)
①红磷过量②装置漏气 ③没有冷却至室温就打开止水夹
(3)实验完毕后,剩余气体主要是氮气;由此可以推测出剩余气体具有哪些化学性质?不支持燃烧;
(4)若将红磷换成木炭,该实验能否获得成功否(填“能”或“否”)?
分析 只有熟悉用红磷测定空气组成的实验原理、操作、现象、结论和注意事项,才能正确解答本题.
解答 解:(1)红磷燃烧时最明显的现象是产生大量白烟;文字表达式为:磷+氧气$\stackrel{点燃}{→}$五氧化二磷;化学方程式为4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;
(2)根据实验现象可以知道红磷燃烧消耗掉氧气,瓶内压强较小,打开弹簧夹,观察到烧杯中的水进入集气瓶,瓶内水面上升约占集气瓶容积的八分之一,该同学测得的空气中氧气的体积分数为$\frac{1}{8}$×100%=12.5%.与理论值21%相比较,产生误差的原因很可能原因是:装置漏气,或红磷不足,或装置未冷却等.
(3)实验完毕后,剩余气体主要是氮气,由此可以推测出氮气不支持燃烧;
(4)若将红磷换成木炭,该实验不能成功,因为碳与氧气反应,消耗氧气,但同时又生成二氧化碳气体,瓶中的压强没有减小;
故答案为:
(1)产生大量白烟;磷+氧气$\stackrel{点燃}{→}$五氧化二磷(4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5)
(2)12.5;②③;
(3)氮气;不支持燃烧;
(4)否.
点评 本题主要考查用红磷测定空气组成的实验原理、操作、现象、结论和注意事项,难度稍大.

练习册系列答案
相关题目
1.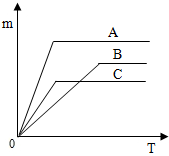 等质量的A、B、C三种金属与足量的稀硫酸反应后生成+2价的硫酸盐,生成氢气的质量(m)与反应时间(T)的关系图如图所示,则下列说法正确的( )
等质量的A、B、C三种金属与足量的稀硫酸反应后生成+2价的硫酸盐,生成氢气的质量(m)与反应时间(T)的关系图如图所示,则下列说法正确的( )
 等质量的A、B、C三种金属与足量的稀硫酸反应后生成+2价的硫酸盐,生成氢气的质量(m)与反应时间(T)的关系图如图所示,则下列说法正确的( )
等质量的A、B、C三种金属与足量的稀硫酸反应后生成+2价的硫酸盐,生成氢气的质量(m)与反应时间(T)的关系图如图所示,则下列说法正确的( )| A. | 三种金属的相对原子量是A<C<B | B. | 三种金属的活泼性是A>B>C | ||
| C. | 反应消耗硫酸的质量相同 | D. | 反应速度最快的是A,最慢的是B |
6.近年来汽车轮胎中常以空气中含量最多的气体作为填充气,这种气体是( )
| A. | 氧气 | B. | 稀有气体 | C. | 二氧化碳 | D. | 氮气 |
20.填写表格:
| (1) | (2) | |||||
| 化学符号 | H | 2P2O5 | Al3+ | 2Fe | O3 | $\stackrel{+2}{C}$O |
| 名称或意义(只写一种) | 氢元素 | 2个五氧化二磷分子 | 铝离子 | 2个铁原子 | 由3个氧原子构成的一个臭氧分子 | 一氧化碳中碳元素显+2价 |

 如图是A、B、C三种固体物质的溶解度曲线,请根据曲线回答:
如图是A、B、C三种固体物质的溶解度曲线,请根据曲线回答: ;(4)两个五氧化二磷分子2P2O5.
;(4)两个五氧化二磷分子2P2O5.