题目内容
20.现有一瓶标签已破损的过氧化氢溶液,为测定瓶内溶液中溶质的质量分数,取该溶液34g于烧杯中,加入2g二氧化锰,完全反应后,称得烧杯内剩余物质的总质量是35.2g.请根据要求回答下列问题:(1)发生反应的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(2)生成氧气的质量是0.8克;
(3)根据生成的氧气的质量,列出求发生分解的过氧化氢质量(x)的比例式为$\frac{68}{32}=\frac{x}{0.8g}$
(4)瓶内过氧化氢溶液中溶质的质量分数是5%.
分析 (1)熟记常用的化学方程式.
(2)根据质量守恒定律,反应前后减少的质量为氧气的质量.
(3)过氧化氢溶液的质量已知,可根据氧气的质量求出过氧化氢的质量.
(4)过氧化氢溶液中溶质的质量分数=$\frac{过氧化氢的质量}{过氧化氢溶液的质量}$×%,
解答 解:(1)过氧化氢以二氧化锰为催化剂生成水和氧气.故其反应的化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(2)34g+2g-35.2g=0.8g,故生成氧气的质量是为:0.8g.
(3)设过氧化氢溶液中溶质的质量为x.
2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑
68 32
x 0.8g
则$\frac{68}{32}=\frac{x}{0.8g}$,解得x=1.7g.
(4)过氧化氢溶液中溶质的质量分数=$\frac{1.7g}{34g}×100$%=5%.
答:过氧化氢溶液中溶质的质量分数为5%.
故答案为:
(1)2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;(2)0.8;(3)$\frac{68}{32}=\frac{x}{0.8g}$;(4)5%.
点评 本题为最基本的根据化学方程式的计算题,解答本题的关键是根据质量守恒定律求出氧气的质量.

练习册系列答案
 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案
相关题目
11.下列物质的用途主要利用其化学性质的是( )
| A. | 干冰用于人工降雨 | B. | 氧气用于医疗急救 | ||
| C. | 活性炭用于除臭味和色素 | D. | 洗洁精用于餐具去油 |
15.在某H2O2溶液中氢元素与氧元素的质量比为2:23,现向2.5g该H2O2溶液中加入0.5g二氧化锰,充分反应后,生成氧气的质量为( )
| A. | 0.4g | B. | 0.5g | C. | 0.6g | D. | 0.7g |
1.在一次关于金属的实验探究中,化学兴趣小组同学做了如下实验记录:
Ⅰ.将相同质量的镁粉和金属X的粉末分别加入到相同质量、相同浓度而且足量的稀硫酸中充分反应,生成氢气的体积V和溶液温度T与时间t的关系分别如图一和图二所示.

Ⅱ.将一定量镁粉和金属X的粉末加入到硫酸铜溶液中,有气泡产生;充分反应后过滤,得到固体甲和无色溶液乙.将固体甲加入到稀硫酸中,有气泡产生.
根据实验记录Ⅰ和Ⅱ分析,有如下说法:
(1)化学反应伴随能量变化.
(2)相同条件下,镁比X与稀硫酸反应更剧烈.
(3)在金属活动性顺序表中,镁和X都排在氢之前.
(4)镁粉和金属X的粉末加入到硫酸铜溶液中有气泡产生属于偶然现象.
(5)固体甲中肯定有铜和X,可能有镁;无色溶液乙中肯定有硫酸镁,肯定没有硫酸铜.
其中一定正确的是( )
Ⅰ.将相同质量的镁粉和金属X的粉末分别加入到相同质量、相同浓度而且足量的稀硫酸中充分反应,生成氢气的体积V和溶液温度T与时间t的关系分别如图一和图二所示.

Ⅱ.将一定量镁粉和金属X的粉末加入到硫酸铜溶液中,有气泡产生;充分反应后过滤,得到固体甲和无色溶液乙.将固体甲加入到稀硫酸中,有气泡产生.
根据实验记录Ⅰ和Ⅱ分析,有如下说法:
(1)化学反应伴随能量变化.
(2)相同条件下,镁比X与稀硫酸反应更剧烈.
(3)在金属活动性顺序表中,镁和X都排在氢之前.
(4)镁粉和金属X的粉末加入到硫酸铜溶液中有气泡产生属于偶然现象.
(5)固体甲中肯定有铜和X,可能有镁;无色溶液乙中肯定有硫酸镁,肯定没有硫酸铜.
其中一定正确的是( )
| A. | (1)(2)(3)(5) | B. | (2)(3)(4) | C. | (3)(4)(5) | D. | (1)(3)(5) |
5.向一定质量的AgNO3和Fe(NO3)2的混合溶液中加入X克Zn粉,充分反应后过滤,将滤渣洗涤、干燥后称量,得到的固体质量仍为X克.下列说法错误的是( )
| A. | 滤液有两种可能的组成 | |
| B. | 滤液中滴加稀盐酸,有白色沉淀产生 | |
| C. | 滤渣中至少有两种物质 | |
| D. | 滤渣中滴加稀盐酸,一定有气泡产生 |
6.如表是NaCl、NH4Cl、KNO3的部分溶解度,请回答下列问题.
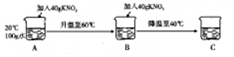
(1)20℃时,溶解度最大的物质是NH4Cl.
(2)按如图所示进行操作(每步均充分溶解),可得到饱和溶液的有AC(填字母),溶质质量分数最大的是B(填字母).

| 温度(℃) | 20 | 40 | 50 | 60 | 80 | |
| 溶解度(g/100g水) | NaCl | 36.0 | 36.6 | 37.0 | 37.3 | 38.4 |
| NH4Cl | 37.2 | 45.8 | 50.4 | 55.2 | 65.6 | |
| KNO3 | 31.6 | 63.9 | 85.5 | 110 | 169 | |
(2)按如图所示进行操作(每步均充分溶解),可得到饱和溶液的有AC(填字母),溶质质量分数最大的是B(填字母).
