题目内容
2.现有一块合金,其质量为35克,使它与足量稀硫酸完全反应后,生成氢气2克,则此合金的组成元素应为( )| A. | Zn和Fe | B. | Zn和Al | C. | Mg和Al | D. | Fe和Cu |
分析 首先判断金属能否与酸反应,然后从金属与酸反应生成氢气的质量关系考虑.根据化学方程式,可得出如下金属与氢气的质量关系:Mg-H2:24-2 Al-H2:18-2 Fe-H2:56-2 Zn-H2:65-2;利用平均值法:A 金属的数值<混合物金属的数值<金属B的数值.
解答 解:根据化学方程式已知金属与氢气的质量关系:Mg-H2:24-2 Al-H2:18-2 Fe-H2:56-2 Zn-H2:65-2;利用平均值生成1克氢气应该符合:A 金属的数值<17.5<金属B的数值.
A、65和56均大于35,不可能;
B、18g<35g<65g,可能;
C、24和18均小于35,不可能;
D、铜不参与反应,56g>35g,不可能.
故选B.
点评 记住记住常见金属与酸反应生成氢气的质量比,对解决此类题目很有帮助.

练习册系列答案
相关题目
4.某同学发现,上个月做实验用的氢氧化钠溶液忘记了盖瓶盖.对于该溶液是否变质,同学们做出了如下假设:
假设一:该溶液没有变质,溶质只有氢氧化钠;
假设二:该溶液部分变质,溶质有氢氧化钠和碳酸钠两种;
假设三:该溶液全部变质,溶质只有碳酸钠.
(1)请帮助这位同学完成以下探究.
写出有白色沉淀反应的化学方程式:Na2CO3+CaCl2═CaCO3↓+2NaCl.
【实验反思】(2)、请你再设计一个实验,验证假设一正确.
(3)(1)的探究实验也有不足,因为实验前未排除氯化钠和氯化钙对酚酞溶液颜色变化的影响.
假设一:该溶液没有变质,溶质只有氢氧化钠;
假设二:该溶液部分变质,溶质有氢氧化钠和碳酸钠两种;
假设三:该溶液全部变质,溶质只有碳酸钠.
(1)请帮助这位同学完成以下探究.
| 实验步骤 | 可能出现的实验现象 | 实验结论 |
| 取少量该溶液于试管中,加入过量氯化钙溶液,静置,取上层清液于另一支试管中,加入几滴酚酞溶液. | ①无白色沉淀生成;②溶液呈红色 | 假设一正确 |
| ①有白色沉淀生成;②酚酞溶液变红 | 假设二正确 | |
| ①白色沉淀生成 ②溶液不变红 | 假设三正确 |
【实验反思】(2)、请你再设计一个实验,验证假设一正确.
| 实验方法 | 实验现象 | 实验结论 |
| 假设一正确 |
5.在一个密闭容器中放入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如表所示:
下列说法不正确的是( )
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前质量/g | 10 | 1 | 2 | 38 |
| 反应后质量/g | 42 | 5 | X(未知) | 2 |
| A. | 丁一定是化合物 | B. | 丙可能是该反应的催化剂 | ||
| C. | 该反应的基本类型可能是化合反应 | D. | X的值为2 |
9.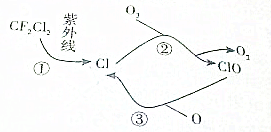 卤代烷烃曾用作冰箱制冷剂,但在高空中与某些气体发生反应,破坏臭氧层,而被逐渐淘汰.如氟氯甲烷(CF2Cl2)在高空中会发生如图所示的变化,根据图示,判断下列说法中不正确的是( )
卤代烷烃曾用作冰箱制冷剂,但在高空中与某些气体发生反应,破坏臭氧层,而被逐渐淘汰.如氟氯甲烷(CF2Cl2)在高空中会发生如图所示的变化,根据图示,判断下列说法中不正确的是( )
 卤代烷烃曾用作冰箱制冷剂,但在高空中与某些气体发生反应,破坏臭氧层,而被逐渐淘汰.如氟氯甲烷(CF2Cl2)在高空中会发生如图所示的变化,根据图示,判断下列说法中不正确的是( )
卤代烷烃曾用作冰箱制冷剂,但在高空中与某些气体发生反应,破坏臭氧层,而被逐渐淘汰.如氟氯甲烷(CF2Cl2)在高空中会发生如图所示的变化,根据图示,判断下列说法中不正确的是( )| A. | ②过程发生的变化是:Cl+O2→ClO+O2 | B. | ③过程发生的变化是:ClO+O→Cl+O2 | ||
| C. | Cl反复作用使O3不断转变为O2 | D. | 氟氯甲烷是上述总反应的催化剂 |
14.下列各组物质能在水溶液中大量共存的是( )
| A. | HCl、NaOH、H2SO4 | B. | AgNO3、HNO3、BaCl2 | ||
| C. | Fe2(SO4)3、NaCl、KOH | D. | FeCl3、Na2SO4、KNO3 |
11.根据所给信息写出相关的化学方程式:
(1)稀盐酸可破坏铝锅表面的氧化膜(主要成分是Al2O3);
(2)胃酸过多时,可服用氢氧化镁药品来减轻症状;
(3)丁烷(C4H10)完全燃烧生成CO2和H2O.
(1)稀盐酸可破坏铝锅表面的氧化膜(主要成分是Al2O3);
(2)胃酸过多时,可服用氢氧化镁药品来减轻症状;
(3)丁烷(C4H10)完全燃烧生成CO2和H2O.
12.元素周期表是学习和研究化学的重要工具.请下表(元素周期表的部分内容)回答有关问题:
(1)请从上表中查出关于硼元素的一条信息:硼的元素符号为B.
(2)第3周期(横行)中属于金属元素的是钠(填一种),其阳离子是Na+(填符号).
(3)第11号元素与第17号元素组成的化合物是NaCl,构成该物质的微粒是离子(填“分子”或“原子”或“离子”).
(4)在元素周期中,同一族(纵行)的元素具有相似的化学性质.则下列各组元素具有相似化学性质的是BD(填字母序号).
A.C和Ne B.Be和Mg C.Al和Si D.F和Cl
(5)元素周期表中每一个横行叫做一个周期,通过分析,同一周期元素之间的排列有一定的规律,如AB(填字母序号).
A.从左到右,各元素原子的电子层数相同
B.从左到右,各元素原子的原子序数依次增加
C.从左到右,各元素原子的最外层电子数相同.
| 周期/族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | 3Li 锂 6.941 | 4Be 铍 9.012 | 5B 硼 10.81 | 6C 碳 12.01 | 7N 氮 14.01 | 8O 氧 16.00 | 9F 氟 19.00 | 10Ne 氖 20.18 |
| 3 | 11Na 钠 22.99 | 12Mg 镁 24.31 | 13Al 铝 26.98 | 14Si 硅 28.09 | 15P 磷 30.97 | 16S 氯 32.06 | 17Cl 氯 35.45 | 18Ar 氩 39.95 |
(2)第3周期(横行)中属于金属元素的是钠(填一种),其阳离子是Na+(填符号).
(3)第11号元素与第17号元素组成的化合物是NaCl,构成该物质的微粒是离子(填“分子”或“原子”或“离子”).
(4)在元素周期中,同一族(纵行)的元素具有相似的化学性质.则下列各组元素具有相似化学性质的是BD(填字母序号).
A.C和Ne B.Be和Mg C.Al和Si D.F和Cl
(5)元素周期表中每一个横行叫做一个周期,通过分析,同一周期元素之间的排列有一定的规律,如AB(填字母序号).
A.从左到右,各元素原子的电子层数相同
B.从左到右,各元素原子的原子序数依次增加
C.从左到右,各元素原子的最外层电子数相同.
