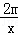题目内容
等质量、等质量分数的两份稀硫酸分别于足量的镁和锌反应,则产生的氢气质量( )
|
| A. | 镁反应得到多 | B. | 锌反应得到多 | C. | 一样多 | D. | 无法确定 |
| 两种二价金属与足量硫酸反应得到氢气多少的计算,可以用归一法计算后分析. | |
| 解答: | 解:足量硫酸,说明金属完全反应. 由于都是二价金属,则设金属为M,相对原子质量为x,生成的氢气的质量为y,金属的质量为m. M+H2SO4=MSO4+H2↑ x 2 m y = y= 即反应得到的氢气的质量与金属的相对原子质量成反比,由于镁的相对原子质量小,所以对应生成的氢气就多; 故选A |

练习册系列答案
相关题目
甲、乙、丙三同学在探究铁与铝在溶液中的活动性强弱时记录的实验报告如下:
| 操 作 | 现 象 | 结 论 与 理 由 |
| 甲、乙同学将铁片、 铝片分别加入到等 体积、等质量分数 的稀硫酸中 | 开始时铁片比铝片反应的 剧烈,过一会后,铝片比 铁片反应剧烈的多,直到 金属片消失。 | 甲同学:铁比铝活动性强 理由是:开始时铁片比铝片反应的剧烈 乙同学:铝比铁活动性强 理由是:过一会后,铝片比铁片反应剧烈 |
| 丙同学将铁粉与 铝片也加入到等 体积、等质量分数 的稀硫酸中 | 铁粉自始至终比铝片反应 的剧烈 | 丙同学:铁比铝活动性强 理由是:铁粉自始至终比铝片反应的剧烈 |
回答:结论正确的是 同学,但该同学的理由说的不完整,请你说明开始铝片比铁片反应慢的原因 ;
丙同学的错误是 。