题目内容
甲、乙、丙三同学在探究铁与铝在溶液中的活动性强弱时记录的实验报告如下:
操作现象结论与理由
甲、乙同学将铁片、铝片分别加入到等体积、等质量分数的稀硫酸中 开始时铁片比铝片反应的剧烈,过一会后,铝片比铁片反应剧烈的多,直到金属片消失. 甲同学:铁比铝活动性强理由是:开始时铁片比铝片反应的剧烈
乙同学:铝比铁活动性强理由是:过一会后,铝片比铁片反应剧烈
丙同学将铁粉与铝片也加入到等体积、等质量分数的稀硫酸中 铁粉自始至终比铝片反应的剧烈 丙同学:铁比铝活动性强理由是:铁粉自始至终比铝片反应的剧烈
回答:结论正确的是
操作现象结论与理由
甲、乙同学将铁片、铝片分别加入到等体积、等质量分数的稀硫酸中 开始时铁片比铝片反应的剧烈,过一会后,铝片比铁片反应剧烈的多,直到金属片消失. 甲同学:铁比铝活动性强理由是:开始时铁片比铝片反应的剧烈
乙同学:铝比铁活动性强理由是:过一会后,铝片比铁片反应剧烈
丙同学将铁粉与铝片也加入到等体积、等质量分数的稀硫酸中 铁粉自始至终比铝片反应的剧烈 丙同学:铁比铝活动性强理由是:铁粉自始至终比铝片反应的剧烈
回答:结论正确的是
乙
乙
同学,但该同学的理由说的不完整,请你说明开始铝片比铁片反应慢的原因铝表面存在氧化铝的保护膜,阻碍了铝与稀盐酸反应的进行
铝表面存在氧化铝的保护膜,阻碍了铝与稀盐酸反应的进行
;丙同学的错误是反应物的颗粒大小不同
反应物的颗粒大小不同
.分析:根据铝易在表面形成氧化铝的保护膜以及反应物的颗粒大小不同其反应的速度不同分析解答;
解答:解:根据金属活动性顺序可知铝的活动性强与铁,所以乙同学说法正确,将铁片、铝片分别加入到等体积、等质量分数的稀硫酸中 开始时铝片反应较慢的原因是铝表面存在氧化铝的保护膜,阻碍了铝与稀盐酸反应的进行,当氧化铝保护膜耗尽时铝片比铁片反应剧烈,丙同学的错误原因是由于两者反应时的颗粒大小不同,从而导致铁粉的反应速度大于铝片;
故答案为:乙;铝表面存在氧化铝的保护膜,阻碍了铝与稀盐酸反应的进行;反应物的颗粒大小不同;
故答案为:乙;铝表面存在氧化铝的保护膜,阻碍了铝与稀盐酸反应的进行;反应物的颗粒大小不同;
点评:本考点主要考查了影响金属与酸发生化学反应速率的因素的探究,主要从金属的活动性和金属的状态等不同的角度,设计实验,也考查了学生的实验设计能力.要认真分析,综合把握,问题就会迎刃而解.本考点主要出现在实验题中;

练习册系列答案
 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案
相关题目
甲、乙、丙三同学在探究铁与铝在溶液中的活动性强弱时记录的实验报告如下:
| 操 作 | 现 象 | 结 论 与 理 由 |
| 甲、乙同学将铁片、 铝片分别加入到等 体积、等质量分数 的稀硫酸中 | 开始时铁片比铝片反应的 剧烈,过一会后,铝片比 铁片反应剧烈的多,直到 金属片消失。 | 甲同学:铁比铝活动性强 理由是:开始时铁片比铝片反应的剧烈 乙同学:铝比铁活动性强 理由是:过一会后,铝片比铁片反应剧烈 |
| 丙同学将铁粉与 铝片也加入到等 体积、等质量分数 的稀硫酸中 | 铁粉自始至终比铝片反应 的剧烈 | 丙同学:铁比铝活动性强 理由是:铁粉自始至终比铝片反应的剧烈 |
回答:结论正确的是 同学,但该同学的理由说的不完整,请你说明开始铝片比铁片反应慢的原因 ;
丙同学的错误是 。
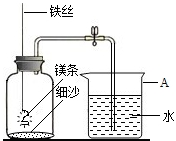 甲、乙、丙三同学在学完了第二单元后,对测定空气中氧气含量的实验非常感兴趣,想探究能否用其它物质来代替红磷完成该实验.他们选取了以下几种物质:铁丝、硫粉、木炭、镁条(镁是一种金属).凭已有知识他们进行了讨论:
甲、乙、丙三同学在学完了第二单元后,对测定空气中氧气含量的实验非常感兴趣,想探究能否用其它物质来代替红磷完成该实验.他们选取了以下几种物质:铁丝、硫粉、木炭、镁条(镁是一种金属).凭已有知识他们进行了讨论: