题目内容
如图所示实验,将稀盐酸滴到含有酚酞试液的氢氧化钠溶液中,直至最终烧杯内溶液呈现无色.则下列说法正确的是( )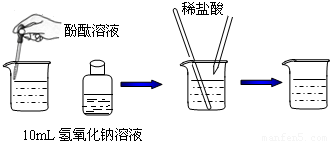
A.酚酞使氢氧化钠溶液变红色
B.溶液中所有物质均以离子形式存在
C.烧杯内显示无色,说明溶液中一定存在大量H+
D.烧杯内显示无色,说明溶液中溶质一定有氯化钠,可能有氯化氢
【答案】分析:酚酞是常用的酸碱指示剂,遇碱变红,在酸性和中性溶液中不变色.含有酚酞试液的氢氧化钠溶液呈红色,滴入稀盐酸,最终烧杯内溶液呈现无色说明最后的溶液不再呈碱性,可能是中性也可能是酸性.
解答:解:A、变色的是指示剂而不是氢氧化钠,故A错误;
B、盐酸、氢氧化钠以及生成的氯化钠是以离子的形式存在,而溶剂水乙分子的形式存在,故B错误;
C、酚酞在酸性和中性溶液中均为无色,烧杯内显示无色,则溶液可能为中性,也可能为酸性,不能确定一定存在大量H+,故C错误;
D、盐酸和氢氧化钠反应生成氯化钠和水,所以溶液中溶质一定有氯化钠,由于不能确定溶液是中性还是酸性,所以说可能有氯化氢,故D正确,
故选D.
点评:本题考查了酸碱中和反应,可以依据课本已有的知识作出回答,本题的易错点就是指示剂与酸碱混合时的颜色变化是指示剂变色而非酸碱变色.
解答:解:A、变色的是指示剂而不是氢氧化钠,故A错误;
B、盐酸、氢氧化钠以及生成的氯化钠是以离子的形式存在,而溶剂水乙分子的形式存在,故B错误;
C、酚酞在酸性和中性溶液中均为无色,烧杯内显示无色,则溶液可能为中性,也可能为酸性,不能确定一定存在大量H+,故C错误;
D、盐酸和氢氧化钠反应生成氯化钠和水,所以溶液中溶质一定有氯化钠,由于不能确定溶液是中性还是酸性,所以说可能有氯化氢,故D正确,
故选D.
点评:本题考查了酸碱中和反应,可以依据课本已有的知识作出回答,本题的易错点就是指示剂与酸碱混合时的颜色变化是指示剂变色而非酸碱变色.

练习册系列答案
 全能闯关100分系列答案
全能闯关100分系列答案
相关题目
如图所示实验,A为一种无色、无刺激性气味的气体,装置Ⅰ硬质玻璃管中装有1.60克红色粉末B,A、B均属纯净物.有关实验内容如下:
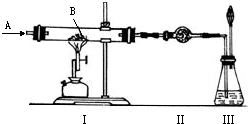
(1)若将所得黑色粉末加入足量稀硫酸中,可生成H20.04克,同时生成一种盐RSO4,则R的相对
原子质量是 .
(2)硬质玻璃管中发生反应的化学方程式是 .
(3)反应后,装置Ⅲ内的液体除沉淀物外,还有的物质是 .
(4)装置Ⅲ处由尖咀管排出的气体,要点火引燃的原因是 .

| 实验内容 | 现象 | 测定结果 |
| ①使A持续地通过实验装置Ⅰ、Ⅱ、Ⅲ | Ⅰ中红色粉末逐渐全部变黑 | Ⅰ中产生的黑色粉末的质量为1.12克 |
| ②当A和B在加热下反应时 | Ⅱ中干燥管里的无水CuSO4无变化 | |
| ③实验完毕时,先移去并熄灭酒精灯,冷至室温后,再停止通A | Ⅲ中澄清石灰水变浑浊 | Ⅲ中沉淀1.00克 |
原子质量是
(2)硬质玻璃管中发生反应的化学方程式是
(3)反应后,装置Ⅲ内的液体除沉淀物外,还有的物质是
(4)装置Ⅲ处由尖咀管排出的气体,要点火引燃的原因是
对比分析是化学研究和学习基本方法.甲、乙、丙三位同学利用如图中的装置,围绕“用称量的方法验证化学反应是否遵守质量守恒定律并分析实验条件”这一探究目的开展活动.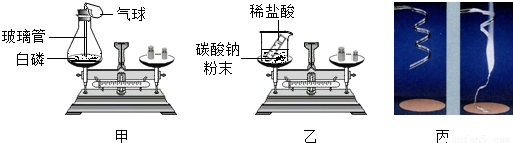
[实验步骤]
①如图所示,甲将白磷和反应装置、乙将装有稀盐酸的小试管和碳酸钠粉末的烧杯,分别放在两个托盘天平上,并用砝码使天平平衡.丙对石棉网和打磨干净的镁条进行称量.
②三位同学分别利用装置进行化学反应.
③甲、乙同学在反应结束且甲的装置冷却后,将反应装置及装置内的物质放在反应前使用的托盘天平上,观察天平是否平衡.丙同学实验结束后称量石棉网和石棉网上氧化镁的质量,比较反应前后质量.
[实验分析]
(1)请你仿照示例,完成实验现象的记录和分析.
(2)比较甲、丙同学的实验有许多相似之处,如生成物都属于下列选项中的 .
A、酸 B、氧化物 C、碱 D、盐
(3)通过对上述实验的对比分析,甲乙两位同学发现丙同学的实验现象是正确的,但结论却是错误的.在实验操作完全正确的情况下,请分析导致丙同学实验前后称量质量不相等的原因有 .
实验结论:化学反应都遵守质量守恒定律.
实验反思:
(4)请从微观角度分析化学反应遵守质量守恒定律的原因是 .

[实验步骤]
①如图所示,甲将白磷和反应装置、乙将装有稀盐酸的小试管和碳酸钠粉末的烧杯,分别放在两个托盘天平上,并用砝码使天平平衡.丙对石棉网和打磨干净的镁条进行称量.
②三位同学分别利用装置进行化学反应.
③甲、乙同学在反应结束且甲的装置冷却后,将反应装置及装置内的物质放在反应前使用的托盘天平上,观察天平是否平衡.丙同学实验结束后称量石棉网和石棉网上氧化镁的质量,比较反应前后质量.
[实验分析]
(1)请你仿照示例,完成实验现象的记录和分析.
| 实验现象 | |||
| 甲同学 | 4P+502 2P2O5 2P2O5 | 该反应遵守质量守恒定律 | |
| 乙同学 | 该反应遵守质量守恒定律 | ||
| 丙同学 | 镁条剧烈燃烧,发出耀眼白光,放热,生成 白色固体.反应前后称量质量不相等. | 该反应不遵守质量守恒定律 |
A、酸 B、氧化物 C、碱 D、盐
(3)通过对上述实验的对比分析,甲乙两位同学发现丙同学的实验现象是正确的,但结论却是错误的.在实验操作完全正确的情况下,请分析导致丙同学实验前后称量质量不相等的原因有 .
实验结论:化学反应都遵守质量守恒定律.
实验反思:
(4)请从微观角度分析化学反应遵守质量守恒定律的原因是 .
如图所示实验,A为一种无色、无刺激性气味的气体,装置Ⅰ硬质玻璃管中装有1.60克红色粉末B,A、B均属纯净物.有关实验内容如下:

(1)若将所得黑色粉末加入足量稀硫酸中,可生成H20.04克,同时生成一种盐RSO4,则R的相对
原子质量是______.
(2)硬质玻璃管中发生反应的化学方程式是______ 2Fe+3CO2

| 实验内容 | 现象 | 测定结果 |
| ①使A持续地通过实验装置Ⅰ、Ⅱ、Ⅲ | Ⅰ中红色粉末逐渐全部变黑 | Ⅰ中产生的黑色粉末的质量为1.12克 |
| ②当A和B在加热下反应时 | Ⅱ中干燥管里的无水CuSO4无变化 | |
| ③实验完毕时,先移去并熄灭酒精灯,冷至室温后,再停止通A | Ⅲ中澄清石灰水变浑浊 | Ⅲ中沉淀1.00克 |
原子质量是______.
(2)硬质玻璃管中发生反应的化学方程式是______ 2Fe+3CO2