题目内容
14.称取12.5g石灰石(主要成分是CaCO3,杂质不参加反应)放人烧杯中,向其中加入50g稀盐酸,二者恰好完全反应.反应结束后称量烧杯中剩余物质的总质量为58.1g(不包括烧杯的质量,且气体的溶解忽略不计).(1)试计算生成CO2的质量为多少?
(2)求石灰石样品中碳酸钙的质量为多少?
(3)石灰石中杂质的质量分数为多少?
分析 碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,反应前后的质量差即为反应生成二氧化碳的质量,根据二氧化碳质量可以计算碳酸钙的质量,进一步可以计算石灰石中杂质的质量分数.
解答 解:(1)生成CO2的质量为:12.5g+50g-58.1g=4.4g,
答:生成了4.4g的二氧化碳.
(2)设石灰石样品中碳酸钙的质量为x,
CaCO3+2HCl═CaCl2+H2O+CO2↑,
100 44
x 4.4g
$\frac{100}{x}$=$\frac{44}{4.4g}$,
x=10g,
答:石灰石样品中碳酸钙的质量为10g.
(3)石灰石中杂质的质量分数为:$\frac{12.5g-10g}{12.5g}$×100%=20%,
答:石灰石中杂质的质量分数为20%.
点评 差量法在计算中的应用很广泛,解答的关键是要分析出物质的质量差与要求的未知数之间的关系,再根据具体的数据求解.

练习册系列答案
相关题目
11. 在医院里给病人输氧时,用到类似下图的装置.下列说法不正确的是( )
在医院里给病人输氧时,用到类似下图的装置.下列说法不正确的是( )
 在医院里给病人输氧时,用到类似下图的装置.下列说法不正确的是( )
在医院里给病人输氧时,用到类似下图的装置.下列说法不正确的是( )| A. | 该装置可以观测氧气输出的快慢 | |
| B. | 能用该装置输氧是因为氧气不易溶于水 | |
| C. | 输送的氧气事先保存在蓝色钢瓶内 | |
| D. | b导管应与供氧的钢瓶相连 |
2.如表列出了除去物质中所含少量杂质的方法,其中错误的是( )
| 选项 | 物质 | 杂质 | 除杂方法 |
| A | CO2 | CO | 点燃 |
| B | MnO2粉 | C粉 | 在空气中充分灼烧 |
| C | FeSO4溶液 | CuSO4溶液 | 加入足量的铁粉,过滤 |
| D | NaCl固体 | 泥沙 | 溶解、过滤、蒸发 |
| A. | A | B. | B | C. | C | D. | D |
9.“太阳能光伏发电”能有效推行“低碳经济”的发展,其最关键的材料是高纯硅(Si).三氯甲硅烷(SiHCl3)还原法是当前制备高纯硅的主要方法,生产流程示意图如下:

下列说法正确的是( )

下列说法正确的是( )
| A. | 三氯甲硅烷(SiHCl3)不属于有机物 | |
| B. | 上述流程中可循环使用的物质是H2、HCl | |
| C. | “精馏”是蒸馏的一种,其原理是利用混合物成分的密度不同 | |
| D. | 从粗硅到SiHCl3(粗)的化学反应方程式为:Si+HCl═SiHCl3+H2 |
19.生活中的下列现象,用分子的相关知识解释不正确的是( )
| A. | 不同的花儿有不同的香味,是因为不同的分子性质不同 | |
| B. | 成熟的榴莲会散发出浓浓的气味,说明分子在不断地运动 | |
| C. | 水沸腾时能掀起壶盖,说明分子大小随温度升高而增大 | |
| D. | 氧气加压后变成液氧,是因为分子间的间隔变小 |
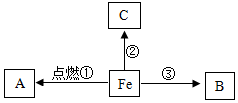 根据如图的转化关系(“→”表示一种物质转化为另一种物质),B是密度最小的气体,C为红色固体单质.请回答下列问题:
根据如图的转化关系(“→”表示一种物质转化为另一种物质),B是密度最小的气体,C为红色固体单质.请回答下列问题:
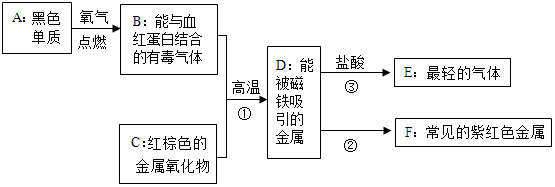
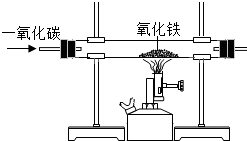 某同学设计了用一氧化碳与氧化铁反应来探究炼铁原理的装置,如图.
某同学设计了用一氧化碳与氧化铁反应来探究炼铁原理的装置,如图.