题目内容
除去下列各组物质中的杂质,所用试剂和方法均正确的是( )
| 物质 | 杂质 | 除杂质所用试剂和方法 | |
| A | H2 | HCl气体 | 先通过足量Na2CO3溶液,再通过浓硫酸 |
| B | KNO3溶液 | AgNO3溶液 | 先加入过量KCl溶液,再过滤 |
| C | KCl固体 | KClO3固体 | 加入少量MnO2加热 |
| D | FeSO4溶液 | CuSO4溶液 | 先加过量Fe粉,再过滤 |
| A、A | B、B | C、C | D、D |
考点:物质除杂或净化的探究,常见气体的检验与除杂方法,盐的化学性质
专题:物质的分离、除杂、提纯与共存问题
分析:根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答:解:A、HCl气体能与足量Na2CO3溶液反应生成氯化钠、水、二氧化碳,能除去杂质但引入了新的杂质二氧化碳,不符合除杂原则,故选项所采取的方法错误.
B、AgNO3溶液能与过量KCl溶液反应生成氯化银白色沉淀和硝酸钾,能除去杂质但引入了新的杂质氯化钾,不符合除杂原则,故选项所采取的方法错误.
C、氯酸钾在二氧化锰的催化作用下生成氯化钾和氧气,二氧化锰作催化剂,反应前后质量不变,能除去杂质但引入了新的杂质二氧化锰,不符合除杂原则,故选项所采取的方法错误.
D、CuSO4溶液能与过量Fe粉反应生成硫酸亚铁溶液和铜,再过滤除去不溶物,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
故选:D.
B、AgNO3溶液能与过量KCl溶液反应生成氯化银白色沉淀和硝酸钾,能除去杂质但引入了新的杂质氯化钾,不符合除杂原则,故选项所采取的方法错误.
C、氯酸钾在二氧化锰的催化作用下生成氯化钾和氧气,二氧化锰作催化剂,反应前后质量不变,能除去杂质但引入了新的杂质二氧化锰,不符合除杂原则,故选项所采取的方法错误.
D、CuSO4溶液能与过量Fe粉反应生成硫酸亚铁溶液和铜,再过滤除去不溶物,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
故选:D.
点评:物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.

练习册系列答案
 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案
相关题目
某固体可能含有氧化钙、氢氧化钙、碳酸钠中的一种或几种.取该固体粉末加足量水溶解,过滤,向滤渣中加稀盐酸有气泡产生.下列关于该固体组成的说法正确的是( )
| A、一定含碳酸钠 |
| B、一定含氢氧化钙 |
| C、一定含氧化钙 |
| D、可能含碳酸钠 |
下列说法不正确的是( )
| A、可以用pH试纸测定正常雨水的pH约为5.6 |
| B、可以用石蕊溶液来确定溶液的酸碱性 |
| C、医疗上可以用氯化钠来配制生理盐水 |
| D、工业上可以用硫酸生产化肥和农药 |
推理是一种重要的研究和学习的方法,下列推理正确的是( )
| A、离子是带电的粒子,则带电的粒子一定是离子 |
| B、氧化物中含有氧元素,则含有氧元素的化合物一定是氧化物 |
| C、某物质燃烧生成CO2和H2O,则该物质中一定含碳、氢元素 |
| D、燃烧一般都伴随发光和放热现象,则有发光和放热现象的变化都是燃烧 |
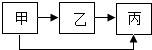 如表所列各组物质中,物质之间按箭头方向通过一步反应不能实现如图所示转化的是
如表所列各组物质中,物质之间按箭头方向通过一步反应不能实现如图所示转化的是| 物质 选项 | 甲 | 乙 | 丙 |
| A | Fe2O3 | CO2 | H2O |
| B | C | CO | CO2 |
| C | CaCO3 | CaO | Ca(OH) 2 |
| D | H2SO4 | H2O | H2 |
| A、A | B、B | C、C | D、D |
20℃时,取甲、乙、丙、丁四种纯净物各40 g,分别加入到四个各盛有100g水的烧杯中,充分溶解,其溶解情况如表:
下列说法正确的是( )
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 未溶解固体的质量/g | 8.4 | 4 | 0 | 18.4 |
| A、所得四杯溶液都是饱和溶液 |
| B、丁溶液的溶质质量分数最大 |
| C、20℃时四种物质溶解度的关系为:丁>甲>乙>丙 |
| D、四杯溶液中各加入20℃的100 g水后,溶液质量相等,且均为不饱和溶液 |