题目内容
某研究小组在实验室制取二氧化碳的研究中发现,通常不选用大理石与稀硫酸反应制取二氧化碳,其原因是反应生成硫酸钙微溶物覆盖在固体的表面,阻碍了大理石与稀硫酸的接触,反应速率逐渐减慢甚至停止.为此,该小组设立研究课题:选择合适浓度的硫酸和适当的反应温度制取二氧化碳.
【实验一】选择合适浓度的硫酸
操作:在28℃时,用装有5mL硫酸溶液的注射器向盛有1g直径为2mm大理石的大试管中注入硫酸,记录15分钟内生成气体的体积,见下表:
①稀硫酸与大理石反应,在28℃时,选用硫酸的浓度最合适为 %,因为浓度小于或大于此浓度对反应的影响是 .
【实验二】选择合适的反应温度
操作:往盛有1g直径为2mm大理石的大试管中分别加入 .观察反应的情况,得出结论.
②在合适的硫酸浓度下,应选择最合适的反应温度为70℃.
③除选用适当的温度和合适浓度的硫酸之外,在反应过程中,为防止硫酸钙覆盖在大理石上,应增加 操作,更有利于气体的制备.
④该研究小组为了研究 对该反应速率的影响,进行了如下实验.
【实验一】选择合适浓度的硫酸
操作:在28℃时,用装有5mL硫酸溶液的注射器向盛有1g直径为2mm大理石的大试管中注入硫酸,记录15分钟内生成气体的体积,见下表:
| 试管编号 | 1 | 2 | 3 | 4 | 5 |
| 硫酸浓度(%) | 15 | 20 | 25 | 30 | 35 |
| 气体体积(mL) | 35 | 47 | 55 | 51 | 42 |
【实验二】选择合适的反应温度
操作:往盛有1g直径为2mm大理石的大试管中分别加入
②在合适的硫酸浓度下,应选择最合适的反应温度为70℃.
③除选用适当的温度和合适浓度的硫酸之外,在反应过程中,为防止硫酸钙覆盖在大理石上,应增加
④该研究小组为了研究
| 试管编号 | A | B |
| 试管内药品 | 1g块状大理石与5mL25%稀硫酸 | 1g粉末状大理石与5mL25%稀硫酸 |
| 现象和比较 | 有少量气泡 | 迅速产生较多气泡 |
考点:制取气体的反应原理的探究,二氧化碳的实验室制法
专题:科学探究
分析:(1)分析实验一中的表格中数据作对比即可得出正确答案;
(2)观察实验二中表格中的数据作对比即可得出正确答案;
(3)为防止硫酸钙覆盖在大理石上,可以用摇动试管的方法解决;
(4)碳酸钙固体颗粒大小也会影响反应的速率,可以据此解答.
(2)观察实验二中表格中的数据作对比即可得出正确答案;
(3)为防止硫酸钙覆盖在大理石上,可以用摇动试管的方法解决;
(4)碳酸钙固体颗粒大小也会影响反应的速率,可以据此解答.
解答:解:【实验一】①观察实验一图表,3号试管收集的气体最多,此时管中硫酸浓度是25%.浓度大于或小于此浓度值生成的气体体积都少.故答案为:25、生成气体体积较少;
【实验二】②根据探究的目的是探究温度对反应的影响,因此可以选择5mL相同合适浓度而不同温度的硫酸溶液,故答案为:5mL相同合适浓度而不同温度的硫酸溶液;
③为防止硫酸钙覆盖在大理石上,可以用摇动试管的方法除去覆盖在大理石上的硫酸钙.
故答案为:搅拌或振荡试管;
④碳酸钙固体颗粒大小也会影响反应的速率,根据表格可知是探究碳酸钙固体颗粒大小;
故答案为:碳酸钙固体颗粒大小.
【实验二】②根据探究的目的是探究温度对反应的影响,因此可以选择5mL相同合适浓度而不同温度的硫酸溶液,故答案为:5mL相同合适浓度而不同温度的硫酸溶液;
③为防止硫酸钙覆盖在大理石上,可以用摇动试管的方法除去覆盖在大理石上的硫酸钙.
故答案为:搅拌或振荡试管;
④碳酸钙固体颗粒大小也会影响反应的速率,根据表格可知是探究碳酸钙固体颗粒大小;
故答案为:碳酸钙固体颗粒大小.
点评:本题以实验探究的形式考查稀硫酸与大理石反应的适宜温度和浓度等问题,培养学生的对比能力、提取信息的能力,注意控制变量的使用.

练习册系列答案
相关题目
下列有关高炉炼铁的说法正确的一组是( )
①高炉中焦炭的作用是产生一氧化碳
②高炉中焦炭的作用是供热
③高炉中把铁矿石冶炼成铁的主要反应原理是2Fe2O3+3C
4Fe+3CO2↑
④高炉炼铁原料有铁矿石、焦炭、石灰石.
①高炉中焦炭的作用是产生一氧化碳
②高炉中焦炭的作用是供热
③高炉中把铁矿石冶炼成铁的主要反应原理是2Fe2O3+3C
| ||
④高炉炼铁原料有铁矿石、焦炭、石灰石.
| A、①②③ | B、②③④ |
| C、①③④ | D、①②④ |
如图是同学们用大可乐瓶(耐酸)设计的储气装置(铁架台未画出),以下说法不正确的是( )

| A、打开止水夹a、b,气体从d管通入,储存在下面的瓶子里,水被压入上瓶 |
| B、取用气体时,打开止水夹a、b,靠水的重力将气体从d管排出 |
| C、该装置也可用于实验室制取二氧化碳的发生装置 |
| D、气体被储存在装置中,c导管也必须安装止水夹 |
室温时,有两瓶硝酸钾溶液,一瓶为饱和溶液(溶质的质量分数为40%)另一瓶为溶质质量分数为10%的溶液.下列实验操作中,无法区分这两种溶液的是( )
| A、加一定量的水 |
| B、加入少量硝酸钾晶体 |
| C、略降低温度 |
| D、室温时,蒸发少量水 |
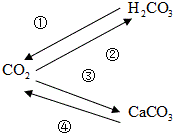 请写出实现下列转化的四个反应的化学方程式:
请写出实现下列转化的四个反应的化学方程式: