题目内容
13.现有碳酸钠和氢氧化钠的混合物18.6g与159.2g稀盐酸恰好完全反应,所得的溶液质量为173.4g.求:(1)反应生成的二氧化碳质量为多少?
(2)所得溶液中溶质质量分数为多少?
分析 碳酸钠与稀盐酸反应生成氯化钠、水和二氧化碳,氢氧化钠与稀盐酸反应生成氯化钠和水,由质量守恒定律,混合物减少的质量即为生成二氧化碳的质量,由反应的化学方程式列式计算出参加反应的碳酸钠的质量、生成氯化钠的质量,进而计算出所得溶液中溶质质量分数即可.
解答 解:(1)由质量守恒定律,生成二氧化碳的质量为18.6g+159.2g-173.4g=4.4g.
(2)设生成氯化钠的质量为x,参加反应的碳酸钠的质量为y,
Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 117 44
y x 4.4g
$\frac{117}{44}=\frac{x}{4.4g}$ x=11.7g
$\frac{106}{44}=\frac{y}{4.4g}$ y=10.6g
则原混合物中含氢氧化钠的质量为18.6g-10.6g=8g.
设与氢氧化钠反应生成氯化钠的质量为z,
HCl+NaOH═NaCl+H2O
40 58.5
8g z
$\frac{40}{58.5}=\frac{8g}{z}$ x=11.7g
所得溶液中溶质质量分数为$\frac{11.7g+11.7g}{173.4g}$×100%≈13.5%.
答:(1)反应生成的二氧化碳质量为4.4g;(2)所得溶液中溶质质量分数为13.5%.
点评 本题难度不大,掌握利用化学方程式与溶质质量分数的综合计算即可正确解答本题,根据质量守恒定律计算出二氧化碳气体的质量是正确解答本题的前提和关键.

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案
相关题目
3.推理是一种非常好的学习方法.下列推理正确的是( )
| A. | 金属能导电,所以能导电的物质一定是金属 | |
| B. | 单质中只含有一种元素,因此只含一种元素的纯净物一定是单质 | |
| C. | CO2和CO都是碳的氧化物,所以它们的化学性质相似 | |
| D. | 化合物是由不同种元素组成的,所以由不同种元素组成的物质一定是混合物 |
4.有甲、乙、丙、丁四种物质,已知甲和乙通常都是无色液体且组成元素相同,甲中加入少量黑色粉末状的丙物质能产生气体A和乙物质,且反应前后丙的质量和化学性质没有改变;丁通常为无色有剧毒的气体,它在A中燃烧生成一种能使澄清石灰水变浑的气体.则下列有关说法错误的是( )
| A. | 甲、乙分别是双氧水和水 | B. | 丙可能是一种氧化物 | ||
| C. | 气体A可能是二氧化碳 | D. | 丁物质是煤气的主要成分 |
18.除去二氧化碳中的水蒸气,可选用的干燥剂是( )
| A. | 氢氧化钠固体 | B. | 生石灰 | C. | 浓硫酸 | D. | 氧化铜 |
18.小李以“百崧河水污染情况调查”为研究课题,为了比较准确地测定百崧河水样品的酸碱度,你建议他使用( )
| A. | 紫色石蕊试液 | B. | 蓝色石蕊试纸 | C. | 无色酚酞试液 | D. | pH试纸 |
19.表中的知识归纳,完全正确的一组是( )
| A.物质的分类 | B.生活中的化学 |
| ①合成纤维、合金都属于合成材料 ②含氧元素的化合物都属于氧化物 ③混合物中一定含有多种元素 | ①吹灭蜡烛--隔绝空气 ②洗涤剂可以除油污--洗涤剂可以使油污乳化 ③用燃烧法鉴别真假羊毛--燃烧的现象不同 |
| C.“低碳经济”的措施 | D.用“化学”眼光分析 |
| ①改造或淘汰高能耗、高污染产业 ②研制和开发新能源替代传统能源 ③优化建筑设计,采光多用自然光 | ①硬水和软水都属于溶液 ②催化剂都加快化学反应速率 ③花香四溢说明分子在不停的运动 |
| A. | A | B. | B | C. | C | D. | D |
 和●分别代表两种不同元素的原子,这两种元素组成的化合物在一定条件下能发生以下反应,反应前后的微观模拟图如下:
和●分别代表两种不同元素的原子,这两种元素组成的化合物在一定条件下能发生以下反应,反应前后的微观模拟图如下: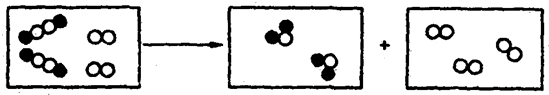
 与
与 的个数比为2:1
的个数比为2:1 代表氧原子,完成上述变化的化学式表达式:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑
代表氧原子,完成上述变化的化学式表达式:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑