��Ŀ����
ͬѧ�����ס��������кͷ�Ӧʵ���̽������ͼ��ʾ��

��1����ʵ��ǡ���кͣ������Һ�е������� ���ѧʽ����
��2��ȡ�ҷ�Ӧ�����Һ60.0g���μ���������26.5%��Na2CO3��Һ����ͼ������ҺpH�ı仯��ͼ��������
CaCl2��Ӧ��̼������Һ������Ϊ g����������Һ��CaCl2��������������Ϊ ��д��������̣���ȷ��0.1%����

��3�����ݼ�������������ͼ���л����������������ߣ�
��4��������кͷ�Ӧ������ƴ��ڵIJ����� ��

��1����ʵ��ǡ���кͣ������Һ�е�������
��2��ȡ�ҷ�Ӧ�����Һ60.0g���μ���������26.5%��Na2CO3��Һ����ͼ������ҺpH�ı仯��ͼ��������
CaCl2��Ӧ��̼������Һ������Ϊ

��3�����ݼ�������������ͼ���л����������������ߣ�
��4��������кͷ�Ӧ������ƴ��ڵIJ�����
���㣺�кͷ�Ӧ����Ӧ��,�й��������������ļ���,��Һ���������pHֵ�Ĺ�ϵ,���ݻ�ѧ��Ӧ����ʽ�ļ���
ר�⣺�������� ���ͨ��
��������1������������������Ƶķ�Ӧ���з�����
��2����Ӧ�����Һ���Ȼ�����Һ����̼������Һ��Ӧ����̼��Ƴ��������ݻ�ѧ��Ӧ����ʽ���з������㣻
��3�����ݼ������ݻ�������ͼ���ɣ�
��4��������кͷ�Ӧ������û�мӷ�̪��Һ������֤�Ƿ�ǡ���кͣ�
��2����Ӧ�����Һ���Ȼ�����Һ����̼������Һ��Ӧ����̼��Ƴ��������ݻ�ѧ��Ӧ����ʽ���з������㣻
��3�����ݼ������ݻ�������ͼ���ɣ�
��4��������кͷ�Ӧ������û�мӷ�̪��Һ������֤�Ƿ�ǡ���кͣ�
����⣺��1��������������Ƶķ�Ӧ�����Ȼ��ƺ�ˮ��ǡ���кͺ���Һ�е�����ֻ���Ȼ��ƣ��ʴ�Ϊ��CaCl2��
��2����ͼ��֪��̼������Һ������70gʱ����Ӧ������ɣ��Ȼ��ƺ�̼���Ƶķ�Ӧ����̼��ƺ�ˮ�������⣬��μӷ�Ӧ��CaCl2������Ϊ x����
CaCl2+Na2CO3=CaCO3��+2NaCl
111 106
x 40g��26.5%
=
��ã�x=11.1g
��CaCl2��Һ��������������Ϊ��
��100%��18.5%
�ʴ�Ϊ��40��18.5%��
��3����ͼ����֪�ҷ�Ӧ�����ҺpH��7��˵����Һ������ϡ���ᣬֱ���μӵ�Na2CO3��Һ�ﵽ30.0g��ϡ���ᱻ��ȫ��Ӧ����Na2CO3��Һ��ʼ��CaCl2��Һ��Ӧ�����μ�Na2CO3��Һ��70.0gʱ��CaCl2��Һ����ȫ��Ӧ����
�裺�μ���������26.5%��Na2CO3��Һ70gʱ����ʱ��CaCl2��Һ��Ӧ��Na2CO3��Һ����Ϊ40g�������ɳ���������Ϊx����
CaCl2+Na2CO3=CaCO3��+2NaCl
106 100
40g��26.5% x
=
��ã�x=10.0g��

��4��������кͷ�Ӧ������û�мӷ�̪��Һ������֤�Ƿ�ǡ���кͣ�
�ʴ�Ϊ������֤�Ƿ�ǡ���кͣ�
��2����ͼ��֪��̼������Һ������70gʱ����Ӧ������ɣ��Ȼ��ƺ�̼���Ƶķ�Ӧ����̼��ƺ�ˮ�������⣬��μӷ�Ӧ��CaCl2������Ϊ x����
CaCl2+Na2CO3=CaCO3��+2NaCl
111 106
x 40g��26.5%
| 111 |
| 106 |
| x |
| 40g��26.5% |
��ã�x=11.1g
��CaCl2��Һ��������������Ϊ��
| 11.1g |
| 60g |
�ʴ�Ϊ��40��18.5%��
��3����ͼ����֪�ҷ�Ӧ�����ҺpH��7��˵����Һ������ϡ���ᣬֱ���μӵ�Na2CO3��Һ�ﵽ30.0g��ϡ���ᱻ��ȫ��Ӧ����Na2CO3��Һ��ʼ��CaCl2��Һ��Ӧ�����μ�Na2CO3��Һ��70.0gʱ��CaCl2��Һ����ȫ��Ӧ����
�裺�μ���������26.5%��Na2CO3��Һ70gʱ����ʱ��CaCl2��Һ��Ӧ��Na2CO3��Һ����Ϊ40g�������ɳ���������Ϊx����
CaCl2+Na2CO3=CaCO3��+2NaCl
106 100
40g��26.5% x
| 106 |
| 100 |
| 40g��26.5% |
| x |
��ã�x=10.0g��

��4��������кͷ�Ӧ������û�мӷ�̪��Һ������֤�Ƿ�ǡ���кͣ�
�ʴ�Ϊ������֤�Ƿ�ǡ���кͣ�
������������һ���ۺ��Ե����ͣ�����Һ����ѧ��Ӧ��ͼ���ں���һ����һ�����Ѷȣ�Ҫ��Ƚϸߣ�ͨ��ѧ���ڼ���ʱ�����������ʵ�ʲμӷ�Ӧ������Һ�����ʵ��������������������ֱ�Ӵ��뻯ѧ����ʽ���м��㣮���Ҫ��ѧ���㹻ϸ�ġ��������������������

��ϰ��ϵ�д�
 �ִʾ�ƪ��ͬ�����Ĵ��ϵ�д�
�ִʾ�ƪ��ͬ�����Ĵ��ϵ�д� �߽�������ϵ�д�
�߽�������ϵ�д�
�����Ŀ
����ʵ�������ȷ���ǣ�������
A�� ����Һ��pHֵ |
B�� ���� |
C�� ��������� |
D�� �㵹Һ�� |
���������������ǣ�������
| A����ij�����еμ�ϡ���ᣬ�����ݲ������ù���һ���ǻ��ý��� |
| B����ij�����м���ʯ����ĥ����ʹʪ��ĺ�ɫʯ����ֽ����������������һ������� |
| C��ij�����������г��ȼ��ֻ���ɶ�����̼��ˮ�����������һ������̼���⡢������Ԫ�� |
| D��pH��7��ij��ɫ��Һһ���Ǽ����Һ |

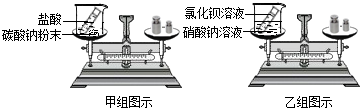
 ��������;ʮ�ֹ㷺����ѧС��Ϊ����ʵ���ҷ�Һ������������������ͭ���е�ͭ���������ͼ��ʵ�鷽����������п��ǡ����ȫ��Ӧ��
��������;ʮ�ֹ㷺����ѧС��Ϊ����ʵ���ҷ�Һ������������������ͭ���е�ͭ���������ͼ��ʵ�鷽����������п��ǡ����ȫ��Ӧ��