题目内容
5. 某溶液可能是由HCl、H2SO4、K2CO3、MgCl2中的一种或几种物质组成,若向该溶液中加入Ba(OH)2溶液时,产生的沉淀与加入Ba(OH)2溶液的质量关系如图所示,则
某溶液可能是由HCl、H2SO4、K2CO3、MgCl2中的一种或几种物质组成,若向该溶液中加入Ba(OH)2溶液时,产生的沉淀与加入Ba(OH)2溶液的质量关系如图所示,则(1)原溶液中含有的溶质是HCl和MgCl2
(2)产生沉淀的化学方程式MgCl2+Ba(OH)2=Mg(OH)2↓+BaCl2.
分析 根据硫酸根离子和钡离子一接触就会生成硫酸钡沉淀,加入一定量的氢氧化钡后才会出现沉淀,所以溶液中一定不含硫酸,一定含有盐酸,盐酸和碳酸钾反应生成氯化钾、水和二氧化碳,所以一定不含碳酸钾,一定含有氯化镁等知识进行分析.
解答 解:(1)硫酸根离子和钡离子一接触就会生成硫酸钡沉淀,加入一定量的氢氧化钡后才会出现沉淀,所以溶液中一定不含硫酸,一定含有盐酸,盐酸和碳酸钾反应生成氯化钾、水和二氧化碳,所以一定不含碳酸钾,一定含有氯化镁,所以原溶液中含有的溶质是:HCl和MgCl2;
(2)产生沉淀的反应是氢氧化钡和氯化镁反应生成氢氧化镁沉淀和氯化钡,化学方程式为:MgCl2+Ba(OH)2=Mg(OH)2↓+BaCl2.
故答案为:(1)HCl和MgCl2;
(2)MgCl2+Ba(OH)2=Mg(OH)2↓+BaCl2.
点评 在解此类题时,首先分析题中所给物质的性质和两两之间的反应,然后依据题中的现象判断各物质的存在性,最后进行验证即可.

练习册系列答案
相关题目
16.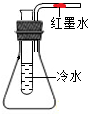 如图所示,导管内有一段红墨水,试管中盛有适量的冷水,容器的气密性良好.现往试管中加入下列某种物质,红墨水不会移动的是( )
如图所示,导管内有一段红墨水,试管中盛有适量的冷水,容器的气密性良好.现往试管中加入下列某种物质,红墨水不会移动的是( )
 如图所示,导管内有一段红墨水,试管中盛有适量的冷水,容器的气密性良好.现往试管中加入下列某种物质,红墨水不会移动的是( )
如图所示,导管内有一段红墨水,试管中盛有适量的冷水,容器的气密性良好.现往试管中加入下列某种物质,红墨水不会移动的是( )| A. | 氢氧化钠固体 | B. | 生石灰 | C. | 浓硫酸 | D. | 蔗糖 |
13.下列有关盐酸叙述错误的是( )
| A. | 打开盛有浓盐酸的试剂瓶瓶塞,在瓶口出现白雾 | |
| B. | 稀盐酸可用于除铁锈 | |
| C. | 浓盐酸可用来干燥氧气 | |
| D. | 在稀盐酸滴加氢氧化钡溶液,出现白色沉淀 |
20.根据你的生活经验和所学的化学知识,判断下列做法正确的是( )
| A. | 用钢丝球洗刷铝锅脏物 | |
| B. | 用洗洁精洗去餐具上的油污,是因为它具有乳化作用 | |
| C. | 铵态氮肥与熟石灰混合使用可以明显提高肥效 | |
| D. | 为减少“白色污染”,应将废弃塑料制品随地焚烧 |
10.氢氧化钠可作干燥剂,但不能用它干燥的气体是:①CO ②CO2③H2④SO2⑤O2 ⑥H2S( )
| A. | ①② | B. | ③④ | C. | ④⑤⑥ | D. | ②④⑥ |
15.下列关于“颜色”说法不正确的是( )
| A. | 无水硫酸铜遇水变成了蓝色 | |
| B. | FeCl3溶液中滴入NaOH溶液出现蓝色沉淀 | |
| C. | 氧化铜和稀硫酸微热出现蓝色溶液 | |
| D. | 在馒头上滴加碘液,碘液变成了蓝色 |

