题目内容
实验室要制取4.4g二氧化碳需要多少克碳酸钙与足量的稀盐酸反应?
解:设需CaCO3的质量为x.
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
x 4.4g
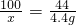
解得 x=10g
答:需CaCO3的质量为10g.
分析:根据碳酸钙与盐酸反应的方程式,由二氧化碳的质量可以求出碳酸钙的质量.
点评:本题主要考查有关化学方程式的计算,难度较小,注意解题的步骤要齐全,格式要规范.
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
x 4.4g
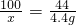
解得 x=10g
答:需CaCO3的质量为10g.
分析:根据碳酸钙与盐酸反应的方程式,由二氧化碳的质量可以求出碳酸钙的质量.
点评:本题主要考查有关化学方程式的计算,难度较小,注意解题的步骤要齐全,格式要规范.

练习册系列答案
相关题目