题目内容
某物质在氧气中燃烧,肯定能出现的现象是( )
| A、发出白光 | B、生成气体 |
| C、有明亮的火焰 | D、放出热量 |
考点:氧气的化学性质
专题:氧气、氢气的性质与用途
分析:根据常见物质在氧气中燃烧的现象进行分析判断.
解答:解:A、物质在氧气中燃烧不一定发出白光,例如铁丝燃烧,故错误;
B、物质在氧气中燃烧不一定生成气体,例如镁条燃烧,故错误;
C、物质在氧气中燃烧不一定有明亮的火焰,例如铁丝燃烧,故错误;
D、燃烧是剧烈的发光、发热的氧化反应,因此物质在氧气中燃烧一定放出热量,故正确.
故选:D.
B、物质在氧气中燃烧不一定生成气体,例如镁条燃烧,故错误;
C、物质在氧气中燃烧不一定有明亮的火焰,例如铁丝燃烧,故错误;
D、燃烧是剧烈的发光、发热的氧化反应,因此物质在氧气中燃烧一定放出热量,故正确.
故选:D.
点评:本题难度不大,掌握常见物质燃烧的现象即可正确解答;在描述物质燃烧的现象时,需要注意光和火焰、烟和雾、实验结论和实验现象的区别.

练习册系列答案
相关题目
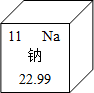 根据如图提供的信息判断,下列说法正确的是( )
根据如图提供的信息判断,下列说法正确的是( )| A、1个钠原子中有11个中子 |
| B、钠的原子序数为11 |
| C、钠属于非金属元素 |
| D、钠的相对原子质量是22.99g |
下列符号既能表示一种元素,又能表示一个原子,还能表示一种单质的是( )
| A、H2 |
| B、H |
| C、Al3+ |
| D、Ag |
密闭容器内有A、B、C、D四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下表,下列说法不正确的是( )
| 物 质 | A | B | C | D |
| 反应前质量/g | 10 | 10 | 10 | 10 |
| 反应后质量/g | 待测 | 12 | 12 | 3 |
| A、反应后密闭容器中A的质量为13g |
| B、该反应一定是分解反应 |
| C、物质D一定是化合物 |
| D、反应生成的A与B的质量之比为13:12 |
下列变化属于化学变化,并且能用质量守恒定律解释的是( )
| A、5g水受热变成5g水蒸气 |
| B、50mL水加入到50mL酒精中,成为体积小于100mL的溶液 |
| C、木炭燃烧后质量减少 |
| D、10g氢气在8g氧气中燃烧最多生成9g水 |
下列实验操作或作法正确的是( )
| A、用100mL量筒量取8.5mL的水 |
| B、为了不造成浪费,实验剩余的药品放回原瓶 |
| C、把烧杯放在垫有石棉网的铁圈上加热 |
| D、用燃着的酒精灯去点燃另一酒精灯 |
主族元素在周期表中的位置取决于该元素的( )
| A、相对原子质量和核外电子数 |
| B、电子层数和最外层电子数 |
| C、相对原子质量的最外层电子数 |
| D、电子层数和次外层电子数 |