题目内容
为了测定某铜锌合金(即铜锌混合物)中锌的质量分数,某同学利用该合金与稀硫酸反应,进行了三次实验,所得相关的实验数据记录如下(实验中的误差忽略不计):
| 第一次 | 第二次 | 第三次 | |
| 所取合金的质量/g | 25 | 25 | 25 |
| 所用稀硫酸的质量/g | 80 | 120 | 160 |
| 生成氢气的质量/g | 0.3 | 0.4 | 0.4 |
(2)后两次产生氢气一样多的原因是______;
(3)试计算该合金中锌的质量分数.
解:(1)所用稀硫酸的量不足,导致合金中锌未完全反应.
(2)合金中能反应的锌已反应完,两次所取合金的质量相等.
(3)设该合金中锌的质量为 X.
Zn+H2SO4═ZnSO4+H2↑
65 2
X 0.4g
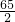 ═
═ ,x=13g
,x=13g
13g÷25×100%═52%
答:合金中锌的质量分数为52%.
分析:由金属与酸反应的条件知道,锌与酸反应,而铜不与酸反应.由表格提供的信息可知,第二次和第三次锌反应完了.再根据反应方程式找出锌与氢气的质量比,由生成氢气的质量可以求出该合金中锌的质量,从而可以求出该合金中锌的质量分数.
点评:解此类题需根据题意正确判断各量之间的准确关系,主要考查了学生分析问题,解决问题的能力.
(2)合金中能反应的锌已反应完,两次所取合金的质量相等.
(3)设该合金中锌的质量为 X.
Zn+H2SO4═ZnSO4+H2↑
65 2
X 0.4g
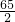 ═
═ ,x=13g
,x=13g13g÷25×100%═52%
答:合金中锌的质量分数为52%.
分析:由金属与酸反应的条件知道,锌与酸反应,而铜不与酸反应.由表格提供的信息可知,第二次和第三次锌反应完了.再根据反应方程式找出锌与氢气的质量比,由生成氢气的质量可以求出该合金中锌的质量,从而可以求出该合金中锌的质量分数.
点评:解此类题需根据题意正确判断各量之间的准确关系,主要考查了学生分析问题,解决问题的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
为了测定某铜锌合金的组成,某校化学课外活动小组利用该合金粉末与稀硫酸反应,进行了三次实验,所得相关的实验数据记录如下:
(1)写出有关反应的化学方程式;
(2)从上表数据分析,当所取合金与所用稀硫酸的质量比为 时,表明合金中的锌与稀硫酸恰好完全反应.(提示:铜与稀硫酸不反应)
(3)试计算该铜锌合金中锌的质量分数.
(4)计算当所用合金与稀硫酸恰好完全反应时,所得溶液中溶质的质量分数.
| 第一次 | 第二次 | 第三次 | |
| 所取合金的质量/g | 10 | 10 | 20 |
| 所用稀硫酸的质量/g | 50 | 80 | 50 |
| 生成氢气的质量/g | 0.2 | 0.2 | 0.2 |
(2)从上表数据分析,当所取合金与所用稀硫酸的质量比为
(3)试计算该铜锌合金中锌的质量分数.
(4)计算当所用合金与稀硫酸恰好完全反应时,所得溶液中溶质的质量分数.
为了测定某铜锌合金中锌的质量分数,某同学利用一定量的该合金与稀硫酸反应,进行了三次实验,相关的实验数据记录如下表.
(1)计算该铜锌合金中锌的质量分数.
(2)计算所用稀硫酸中溶质的质量分数.(结果精确到0.1%)
(可能用到的相对原子质量H-1 O-16 S-32 Cu-64 Zn-65)
| 实验 物质用量 |
第一次 | 第二次 | 第三次 |
| 所取合金的质量/g | 10 | 10 | 10 |
| 所用稀硫酸的质量/g | 50 | 100 | 150 |
| 剩余固体质量/g | 3.5 | 3.0 | 3.0 |
(2)计算所用稀硫酸中溶质的质量分数.(结果精确到0.1%)
(可能用到的相对原子质量H-1 O-16 S-32 Cu-64 Zn-65)
为了测定某铜锌合金中铜的质量分数,取合金样品跟稀盐酸反应.三次实验的有关数据如下表:
(1)根据上表中的数据分析,当铜锌合金中的锌与稀盐酸中的HCl恰好完全反应时,合金样品的质量与稀盐酸的质量之比为 .
(2)计算该铜锌合金中铜的质量分数. .
| 实验编号 | 所需合格样品的质量/g | 所取稀盐酸的质量/g | 生成氢气的质量/g |
| 1 | 10.0 | 40.0 | 0.1 |
| 2 | 10.0 | 50.0 | 0.1 |
| 3 | 20.0 | 36.5 | 0.1 |
(2)计算该铜锌合金中铜的质量分数.
 (2013?浦口区一模)Cu与Zn的合金称为黄铜,有优良的导热性和耐腐蚀性,可用作各种仪器零件.
(2013?浦口区一模)Cu与Zn的合金称为黄铜,有优良的导热性和耐腐蚀性,可用作各种仪器零件.