题目内容
甲、乙两同学分别设计了下述两个实验方案,并都认为如果观察到的现象和自己设计的方案一致,即可确定溶液中有SO42-.甲:溶液
| BaCl2溶液 |
| 加足量稀硫酸 |
乙:溶液
| 加足量稀硫酸 |
| BaCl2溶液 |
试评价上述两个方案是否严密,并分别说明理由:
(1)甲同学方案
(2)乙同学方案
分析:在检验硫酸根离子时,为了排除碳酸根离子的干扰,先向溶液中滴加酸,再加氯化钡,若还有沉淀,说明一定含有硫酸根.
解答:解:在甲溶液中滴加氯化钡溶液,若出现沉淀.这种沉淀有可能是碳酸钡也有可能是硫酸钡,若加入稀硫酸时,碳酸钡和硫酸反应,也有沉淀,故甲方案不严密.
在乙溶液中加入稀硫酸先排除碳酸根的干扰,但是由于硫酸根离子的引入,导致加入氯化钡还有沉淀生成无法确定是先前的硫酸根还是后期加入的硫酸根所致,无法说明溶液中含有硫酸根离子.
故答案为:(1)不严密,因为沉淀若是碳酸钡时加稀硫酸沉淀也不溶解.
(2)不严密.加稀硫酸酸无法确定原溶液是否存在硫酸根离子.
在乙溶液中加入稀硫酸先排除碳酸根的干扰,但是由于硫酸根离子的引入,导致加入氯化钡还有沉淀生成无法确定是先前的硫酸根还是后期加入的硫酸根所致,无法说明溶液中含有硫酸根离子.
故答案为:(1)不严密,因为沉淀若是碳酸钡时加稀硫酸沉淀也不溶解.
(2)不严密.加稀硫酸酸无法确定原溶液是否存在硫酸根离子.
点评:在检验硫酸根离子或氯离子时,一定要注意碳酸根离子的干扰,所以要用稀硝酸再加入白色沉淀,检验沉淀是否消失.

练习册系列答案
 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案
相关题目
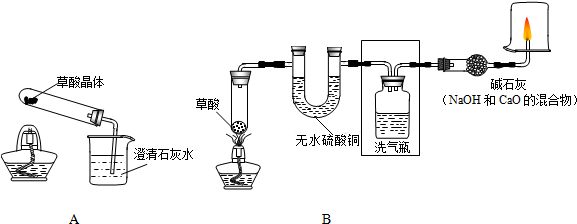
 (2009?石景山区二模)烧碱中常含有碳酸钠.为了测定某烧碱样品中烧碱的质量分数,甲、乙两同学分别设计了如下的实验方案.
(2009?石景山区二模)烧碱中常含有碳酸钠.为了测定某烧碱样品中烧碱的质量分数,甲、乙两同学分别设计了如下的实验方案.