题目内容
【题目】按要求写出下列符号或意义。
(1) 3个硫酸根离子________;
(2)标出氯化亚铁中铁元素的化合价________;
(3) 3NH4+ ________;
(4) 5S2-________;
【答案】3SO42- ![]() 3个铵根离子 5个硫离子
3个铵根离子 5个硫离子
【解析】
(1)由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该离子,就在其离子符号前加上相应的数字,故3个硫酸根离子可表示为:3SO42-;
(2)由化合价的表示方法,在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后,氯化亚铁中铁元素显+2价,故氯化亚铁中铁元素可表示为:![]() ;
;
(3)离子的表示方法:在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该离子,就在其元素符号前加上相应的数字,故3NH4+表示3个铵根离子;
(4)离子的表示方法:在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该离子,就在其元素符号前加上相应的数字,故5S2-表示5个硫离子。

【题目】某同学用镁条测定空气中氧气含量,实验完毕,冷却后进入水的体积远大于总容积的1/5,且产生了淡黄色固体。某兴趣小组对此现象作如下探究。
(问题)为什么会生成淡黄色固体?为什么测得氧气的体积分数会明显偏大?
(资料)镁元素的化合物的颜色:
物 质 | MgO | MgCl2 | Mg3N2 | Mg(NO3)2 | MgCO3 | Mg(OH)2 |
颜 色 | 白色 | 白色 | 淡黄色 | 白色 | 白色 | 白色 |
(猜想)(1)小组成员一致认为产物中一定不含有氯化镁,理由是_______________。
(2)分析资料,小组成员认为淡黄色固体是Mg3N2,是由镁与空气中的_________(填化学式)反应生成的,导致进入水的体积远大于总容积的1/5。该反应的符号表达式是________。
(实验)小组成员设计并进行了下列实验。

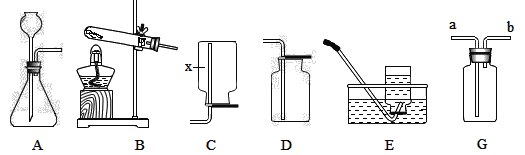
①组装仪器(如下图,钟罩下端无底)。
②将足量白磷在空气中点燃后,迅速伸入钟罩内,塞紧橡皮塞(图1);
③待钟罩内水面不再变化时,向水槽中加水,使水槽中液面与钟罩内液面相平;
④打开橡皮塞,将燃着的螺旋状镁条迅速伸入钟罩内,塞紧橡皮塞(图2);
⑤待钟罩内水面不再变化时,观察到钟罩内壁及表面皿中出现淡黄色固体。
(分析)(3)步骤②中将足量白磷在钟罩内燃烧的目的是__________;钟罩内水面的变化情况_______,
(4)白磷燃烧的符号表达式是_____________。
(5)步骤③中加水的目的是为了防止_______________。
(结论)小组同学的猜想正确。
(拓展)(6)通过以上探究,你对燃烧有什么新认识?请写一点________。
【题目】某校兴趣小组在实验室中完成制取氧气的实验。他们取氯酸钾和二氧化锰的混合物共3.0g放入大试管中加热,并在不同时刻测定试管内剩余固体物质的质量(如下表):分析表中数据,完成下列问题:
反应时间/min | 1.0 | 1.5 | 2.0 | 2.5 | 3.0 |
剩余固体质量g | 2.55 | 2.25 | 2.10 | 2.04 | 2.04 |
(1)完全反应后,生成氧气的质量为_____g
(2)二氧化锰中锰元素的质量分数_____
(3)原混合物中氯酸钾的质量分数是多少_____?(精确到0.1%)