题目内容
高温加热10 g碳酸钙,一段时间后停止加热,测得剩余固体中钙元素的质量分数为50%。
(1)若10 g碳酸钙全部分解可产生多少克氧化钙?
(2)实际反应生成的二氧化碳是多少克?
答案:(1)解:设全部分解可得氧化钙的质量为x。
CaCO3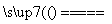 CaO+CO2↑
CaO+CO2↑
100 56
10 g x
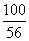 =
=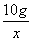 x=5.6 g
x=5.6 g
(2)10 g碳酸钙中钙元素的质量为10 g×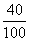 ×100%=4 g
×100%=4 g
反应一段时间后,剩余固体的质量为4 g÷50%=8 g
g
故实际生成CO2的质量为10 g-8 g=2 g
答:(1)全部分解可产生5.6 g氧化钙;(2)实际生成二氧化碳2 g。
解析:(1)由参加反应的碳酸钙的质量,借助化学方程式可求得生成氧化钙的质量;(2)因碳酸钙中钙元素的质量分数小于50%,当完全反应生成氧化钙后,其质量分数大于50%,而此时钙元素质量分数为50%,知:CaCO3未完全分解,可利用在这一过程中“钙元素的质量不变”,求得剩余固体的质量,它们的质量差即为生成二氧化碳的质量。

练习册系列答案
 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案
相关题目
