题目内容
16.操作规范是实验成功的保证,下列图示实验操作中正确的是( )| A. |  读取液体体积 | B. |  过滤 | C. |  倾倒液体 | D. |  放入块状固体 |
分析 本题主要考查化学实验的基本操作,主要从操作要领上来分析.
解答 解:A、读数方法错误,此图为仰视,应视线与凹液面的最低处相平,故A错误.
B、过滤时要用玻璃棒引流,漏斗尖嘴部分紧贴烧杯内壁,故B错误.
C、向试管中倾倒液体时,瓶塞倒放在桌面上,标签向着手心,试管口与试剂瓶口紧挨着,试管要倾斜,故C正确.
D、取用固体药品,首先试管要横放,用纸槽或药匙送到试管底部,故D错误.
故选C.
点评 化学实验的基本操作是做好化学实验的基础,学生要在平时的练习中多操作,掌握操作要领,使操作规范.

练习册系列答案
相关题目
11.下列生活中常见的一些变化,其中属于化学变化的是( )
| A. | 湿衣服晾干 | B. | 花香四溢 | C. | 钢铁生锈 | D. | 木材做成桌椅 |
1.《环境空气质量标准》中的PM2.5指标,是指大气中直径小于或等于2.5微米的颗粒物,下列措施,能减少PM2.5污染的是( )
| A. | 用清洁能源代替化石燃料 | B. | 将生活垃圾焚烧处理 | ||
| C. | 大力发展煤炭火力发电 | D. | 多开私家车出行 |
8.下列除杂方法中,所用试剂合理的是( )
| A. | 用水除去氧化钙中的碳酸钙 | |
| B. | 用氯化钡除去盐酸中混有的稀硫酸 | |
| C. | 用锌粒除去硫酸亚铁中的硫酸铜 | |
| D. | 用氢氧化钡除去碳酸钠中混有的硫酸钠 |
10.工业上常利石灰浆[主要成分为Ca(OH)2]制备化工原料KClO3和超细CaCO3.
Ⅰ.制备KClO3的流程如图1所示:

已知:①反应1为:6Cl2+6Ca(OH)2═Ca(ClO3)2+5CaCl2+6H2O.
②有关物质在常温下的溶解度如表:
(1)操作a的名称是过滤,在实验室中完成此操作需要的玻璃仪器有烧杯、玻璃棒、漏斗,该操作中玻璃棒的作用是引流.
(2)反应2为复分解反应,则溶液A中含有的溶质为CaCl2和KClO3(填化学式),你认为该反应能得到KClO3晶体的原因是相同条件下,氯酸钾的溶解度最小.
(3)洗涤KClO3晶体时,可选用下列C洗涤剂(填字母编号).
A.KCl饱和溶液 B.冰水 C.饱和KClO3溶液
Ⅱ.制备超细CaCO3的流程如图2所示:已知:NH4Cl溶液呈酸性.
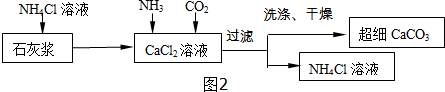
(1)向CaCl2溶液中通入两种气体,生成超细CaCO3的化学方程式CaCl2+H2O+CO2+2NH3═CaCO3↓+2NH4Cl.该流程可循环使用的物质是氯化铵溶液.
(2)检验CaCO3是否洗涤干净的方法是:取最后一次洗涤液,向其中滴加B(填写序号),观察,根据实验现象推断是否洗干净.
A.Na2CO3溶液 B.AgNO3溶液 C.酚酞试液.
Ⅰ.制备KClO3的流程如图1所示:

已知:①反应1为:6Cl2+6Ca(OH)2═Ca(ClO3)2+5CaCl2+6H2O.
②有关物质在常温下的溶解度如表:
| 物质 | Ca(ClO3)2 | CaCl2 | KClO3 | KCl |
| 溶解度/g | 209.0 | 74.5 | 7.3 | 34.2 |
(2)反应2为复分解反应,则溶液A中含有的溶质为CaCl2和KClO3(填化学式),你认为该反应能得到KClO3晶体的原因是相同条件下,氯酸钾的溶解度最小.
(3)洗涤KClO3晶体时,可选用下列C洗涤剂(填字母编号).
A.KCl饱和溶液 B.冰水 C.饱和KClO3溶液
Ⅱ.制备超细CaCO3的流程如图2所示:已知:NH4Cl溶液呈酸性.

(1)向CaCl2溶液中通入两种气体,生成超细CaCO3的化学方程式CaCl2+H2O+CO2+2NH3═CaCO3↓+2NH4Cl.该流程可循环使用的物质是氯化铵溶液.
(2)检验CaCO3是否洗涤干净的方法是:取最后一次洗涤液,向其中滴加B(填写序号),观察,根据实验现象推断是否洗干净.
A.Na2CO3溶液 B.AgNO3溶液 C.酚酞试液.
11.氧化镁在医药、建筑等行业应用广泛,以菱镁矿(主要成分为MgCO3,含少量FeCO3,其他杂质不溶,也不参加反应)为原料制备高纯氧化镁的实验流程如下:
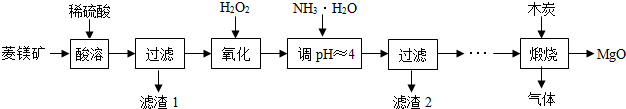
资料:①不同氢氧化物沉淀的pH范围:
②硫在常温下是一种淡黄色固体,硫的熔点约为115.2℃,沸点约为444.7℃;
③高锰酸钾溶液只吸收SO2,不吸收CO2;
④碱溶液既吸收SO2,又吸收CO2.
试回答下列问题:
(1)MgCO3与稀硫酸反应的化学方程式为MgCO3+H2SO4=MgSO4+H2O+CO2↑.
(2)加入H2O2目的是在酸性条件下将FeSO4氧化成Fe2(SO4)3,同时生成水,发生反应的化学方程式为2FeSO4+H2SO4+H2O2=Fe2(SO4)3+2H2O.
(3)加氨水调节溶液的pH约为4的目的是,反应的化学方程式为Fe2(SO4)3+6NH3•H2O=3(NH4)2SO4+2Fe(OH)3↓,过滤后,滤液中含有种阳离子.
(4)煅烧过程存在以下反应:
2MgSO4+C$\frac{\underline{\;800℃\;}}{\;}$2MgO+2SO2↑+CO2↑
MgSO4+C$\frac{\underline{\;800℃\;}}{\;}$MgO+SO2↑+CO↑
MgSO4+3C$\frac{\underline{\;800℃\;}}{\;}$MgO+S↑+3CO↑
利用下图装置对煅烧产生的气体进行分步吸收或收集.(假设每步反应都完全进行)

①A中现象是:玻璃管壁出现色固体;
②B中盛放的溶液可以是d(填字母),实验现象为溶液褪色;
a.Ca(OH)2溶液 b.Na2CO3溶液 c.稀硝酸 d.KMnO4溶液
③C中盛放的溶液可以是氢氧化钠溶液,以吸收CO2气体,D中收集的气体是CO(填化学式).

资料:①不同氢氧化物沉淀的pH范围:
| 氢氧化物 | Fe(OH)3 | Mg(OH)2 |
| 开始沉淀的pH | 1.5 | 8.6 |
| 完全沉淀的pH | 3.2 | 11.1 |
③高锰酸钾溶液只吸收SO2,不吸收CO2;
④碱溶液既吸收SO2,又吸收CO2.
试回答下列问题:
(1)MgCO3与稀硫酸反应的化学方程式为MgCO3+H2SO4=MgSO4+H2O+CO2↑.
(2)加入H2O2目的是在酸性条件下将FeSO4氧化成Fe2(SO4)3,同时生成水,发生反应的化学方程式为2FeSO4+H2SO4+H2O2=Fe2(SO4)3+2H2O.
(3)加氨水调节溶液的pH约为4的目的是,反应的化学方程式为Fe2(SO4)3+6NH3•H2O=3(NH4)2SO4+2Fe(OH)3↓,过滤后,滤液中含有种阳离子.
(4)煅烧过程存在以下反应:
2MgSO4+C$\frac{\underline{\;800℃\;}}{\;}$2MgO+2SO2↑+CO2↑
MgSO4+C$\frac{\underline{\;800℃\;}}{\;}$MgO+SO2↑+CO↑
MgSO4+3C$\frac{\underline{\;800℃\;}}{\;}$MgO+S↑+3CO↑
利用下图装置对煅烧产生的气体进行分步吸收或收集.(假设每步反应都完全进行)

①A中现象是:玻璃管壁出现色固体;
②B中盛放的溶液可以是d(填字母),实验现象为溶液褪色;
a.Ca(OH)2溶液 b.Na2CO3溶液 c.稀硝酸 d.KMnO4溶液
③C中盛放的溶液可以是氢氧化钠溶液,以吸收CO2气体,D中收集的气体是CO(填化学式).
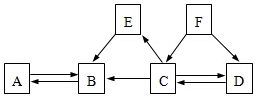 初中化学中几种常见物质之间的相互转化关系如图所示.已知常温下B、C为气体,且B是植物进行光合作用的一种重要原料;D、F均为无色液体,都由两种相同的元素组成,E是黑色固体,与稀硫酸反应得到蓝色溶液(部分反应物和生成物及反应条件已略去).
初中化学中几种常见物质之间的相互转化关系如图所示.已知常温下B、C为气体,且B是植物进行光合作用的一种重要原料;D、F均为无色液体,都由两种相同的元素组成,E是黑色固体,与稀硫酸反应得到蓝色溶液(部分反应物和生成物及反应条件已略去). 用来测定空气成分的方法很多,如图所示的是小明用红磷在空气中燃烧的测定方法.实验过程是:
用来测定空气成分的方法很多,如图所示的是小明用红磷在空气中燃烧的测定方法.实验过程是: