��Ŀ����
С����С��ͬѧѧϰ���ᡢ��κ��֡ü���Һ��ʹ��̪��Һ��죬Na2CO3��ҺҲ��ʹ��̪��Һ��죮����Һʹ��̪��Һ��죬����Ϊ����ˮ�н����OH������ôNa2CO3��Һ�о�������������ʹ��̪��Һ����أ�С���������ͼ����ʵ�飬���㡢С����С��һ��̽����������������

(1)Na2CO3����________(��ᡱ����������Ρ�)��
(2)ʵ������Ŀ����Ϊ��________��
(3)ʵ������������ˮ��Ŀ����̽��ˮ�����Ƿ���ʹ��̪��Һ��죬С��ͬѧ��Ϊʵ����û��Ҫ��������ΪС����������________��
(4)ʵ��������Na2CO3��Һ������̪��Һ��죬��������Һ������εμӹ�����CaCl2��Һ������ɫ����ʧ��ͬʱ���۲쵽������________(��ʾ��CaCl2��Һ������)
��ʵ�������������ó����ۡ���Һ�е�CO32����ʹ��̪��Һ��죻
(5)С��ͬѧ�ں���ʦ������������ʱ����ʦ˵�á���ʵNa2CO3��Һ��ʹ��̪��Һ���Ҳ��������Һ�д���OH����������ΪNa2CO3��Һ�д���OH����ԭ����________��
������
|
�����𰸡�(1)�Σ�(2)̽��Na+�Ƿ���ʹ��̪��Һ��죻(3)��̪��Һ�о���ˮ����(���Ȼ�����Һ�к���ˮ����)��(4)��ɫ������(5)CO32����H2O������Ӧ����OH��(��������)�� ����ר��ÿ�ѧ̽���� ����������(1)������������Ӻ�������ӵĻ��������� ����(2)�Ȼ����к��������ӣ�����̽���������ܷ�ʹ��̪��ɫ�� ����(3)��̪��Һ�о���ˮ���ӻ��Ȼ�����Һ�к��д���ˮ���ӣ�����ʵ����û�б�Ҫ���� ����(4)��Ҫ��̼������Һ���Ȼ�����Һ�ķ�Ӧ���Եó���̼������Ӽ��٣�ʹ��ɫ����ʧ�� ����(5)�����������ܹ�ʹ��̪��죬���Կ����ж���̼������Һ�д������������ӣ� �������� �������(1)̼�����ܵ���������Ӻ�̼������ӣ����������Σ� ����(2)���Ȼ�����Һ�мӷ�̪����ɫ��˵���Ȼ�����Һ�е����Ӷ�����ʹ��̪��죬�������Ӳ���ʹ��̪��ɫ�� ����(3)�Ȼ�����Һ�к��д���ˮ���ӣ���ʵ�����еõ���֤������ʵ������̽���Ƕ���ģ� ����(4)̼������Һ���Ȼ�����Һ��Ӧ����̼��Ƴ�������������Ϊ�����˰�ɫ������ ����(5)����֪��ֻ�����������Ӳ���ʹ��̪��죬������̼������Һ��ʹ��̪��Һ��죬�����ж���Һ�д������������ӣ�Na2CO3��Һ�д���OH����ԭ�������CO32����H2O������Ӧ������OH���� ���������� �������⿼����ѧ�������ṩ��Ϣ���д��������������ʵIJ������ʵ����Ƶ�������Ҫ��ϸߣ�Ҫ��Ϥ����ʵ������˼·�ͷ����� |
��ʾ��
|
�����ʵ��̽�����ʵ����ʻ�仯���ɣ� |

 ��У����ϵ�д�
��У����ϵ�д�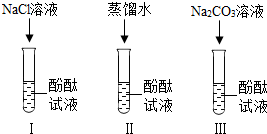 ��2013?��ɳ��С����С��ͬѧѧϰ���ᡢ��κ��֣�����Һ��ʹ��̪��Һ��죬Na2CO3��ҺҲ��ʹ��̪��Һ��죮����Һʹ��̪��Һ��죬����Ϊ����ˮ�н����OH-����ôNa2CO3��Һ�о�������������ʹ��̪��Һ����أ�С���������ͼ����ʵ�飬���㡢С����С��һ��̽��������������⣺
��2013?��ɳ��С����С��ͬѧѧϰ���ᡢ��κ��֣�����Һ��ʹ��̪��Һ��죬Na2CO3��ҺҲ��ʹ��̪��Һ��죮����Һʹ��̪��Һ��죬����Ϊ����ˮ�н����OH-����ôNa2CO3��Һ�о�������������ʹ��̪��Һ����أ�С���������ͼ����ʵ�飬���㡢С����С��һ��̽��������������⣺


 С����С��ͬѧѧϰ���ᡢ��κ��֣�����Һ��ʹ��̪��Һ��죬Na2CO3��ҺҲ��ʹ��̪��Һ��죮����Һʹ��̪��Һ��죬����Ϊ����ˮ�н����OH-����ôNa2CO3��Һ�о�������������ʹ��̪��Һ����أ�С���������ͼ����ʵ�飬���㡢С����С��һ��̽��������������⣺
С����С��ͬѧѧϰ���ᡢ��κ��֣�����Һ��ʹ��̪��Һ��죬Na2CO3��ҺҲ��ʹ��̪��Һ��죮����Һʹ��̪��Һ��죬����Ϊ����ˮ�н����OH-����ôNa2CO3��Һ�о�������������ʹ��̪��Һ����أ�С���������ͼ����ʵ�飬���㡢С����С��һ��̽��������������⣺