题目内容
13.某元素的氧化物化学式为M2O3,其中M元素与氧元素的质量比为7:3.则M相对原子质量是56,此氧化物的化学式是Fe2O3,相对分子质量是160.分析 根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比、相对分子质量为构成分子的各原子的相对原子质量之和,进行分析解答.
解答 解:由题意,某氧化物M2O3中,M与氧元素的质量比是7:3,设元素M的相对原子质量是x,2x:(16×3)=7﹕3,则x=56.此氧化物的化学式为Fe2O3;此相对分子质量为:56×2+16×3=160.
故答案为:56;Fe2O3;160.
点评 本题难度不大,考查同学们灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
相关题目
3.3.0g某物质完全燃烧后生成4.4gCO2和1.8g水.则对该物质相关判断正确的是( )
| A. | 该物质中碳元素的质量分数为40% | |
| B. | 该物质一定含有碳、氢元素,可能含有氧元素 | |
| C. | 该物质由碳、氢、氧元素组成 | |
| D. | 该物质分子中碳原子和氢原子的个数比为1:1 |
4.甲醛(化学式为CH2O)是室内装潢时的主要污染物之一,下列关于甲醛的说法正确的是( )
| A. | 甲醛是由碳、氢、氧三种元素组成的 | |
| B. | 甲醛是由碳原子和水分子构成的 | |
| C. | 甲醛由一个碳原子、两个氢原子、一个氧原子构成 | |
| D. | 甲醛由一个碳元素、两个氢元素、一个氧元素组成的 |
1.下列对分子、原子、离子的认识,正确的是( )
| A. | 原子是最小的粒子,不可再分 | |
| B. | 氮分子是保持氮气化学性质的最小微粒 | |
| C. | 离子不能直接构成物质 | |
| D. | 固体难压缩,说明固体分子间无间隔 |
9.用焊锡进行焊接时,为了清除金属表面的锈,焊接处要滴几滴( )
| A. | 食盐 | B. | 盐酸 | C. | 蒸馏水 | D. | 烧碱 |
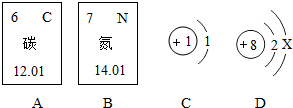 下图A、B是碳元素和氮元素在元素周期表中的部分信息,C、D是两种粒子的结构示意图.仔细观察,按要求回答下列问题:
下图A、B是碳元素和氮元素在元素周期表中的部分信息,C、D是两种粒子的结构示意图.仔细观察,按要求回答下列问题: