题目内容
一氧化碳中混有以下气体中的两种,实验测得该混合气体中含氧元素57%,则该杂质一定不可能是以下的( )①CO2 ②NO ③NO2 ④N2.
A.②③
B.①③
C.①④
D.②④
【答案】分析:根据一氧化碳的化学式可求出其中氧元素的质量分数为: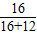 ×100%=57.1%,故杂质中气体中的氧元素的质量分数至少有一种要小于57%进行分析.
×100%=57.1%,故杂质中气体中的氧元素的质量分数至少有一种要小于57%进行分析.
解答:解:二氧化碳中氧元素的质量分数=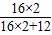 ×100%=72.8%
×100%=72.8%
一氧化氮中氧元素的质量分数=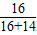 ×100%=53.3%
×100%=53.3%
二氧化氮中氧元素的质量分数=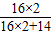 ×100%=69.6%
×100%=69.6%
氮气中没有氧元素,故氧元素的质量分数为0;
A、②③组合中一氧化氮的氧元素质量分数为53.3%,小于57%;故可能为杂质;
B、①③组合中二氧化碳和二氧化氮中氧元素的质量分数都大于57%;故不能为杂质;
C、①④组合中氮气的氧元素的质量分数为0,小于57%;故可能为杂质;
D、②④组合中二者的氧元素质量分数都小于57%,故可能为杂质;
故选B
点评:本题主要考查了元素质量分数的计算,元素的质量分数= ×100%.
×100%.
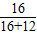 ×100%=57.1%,故杂质中气体中的氧元素的质量分数至少有一种要小于57%进行分析.
×100%=57.1%,故杂质中气体中的氧元素的质量分数至少有一种要小于57%进行分析.解答:解:二氧化碳中氧元素的质量分数=
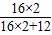 ×100%=72.8%
×100%=72.8%一氧化氮中氧元素的质量分数=
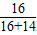 ×100%=53.3%
×100%=53.3%二氧化氮中氧元素的质量分数=
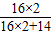 ×100%=69.6%
×100%=69.6%氮气中没有氧元素,故氧元素的质量分数为0;
A、②③组合中一氧化氮的氧元素质量分数为53.3%,小于57%;故可能为杂质;
B、①③组合中二氧化碳和二氧化氮中氧元素的质量分数都大于57%;故不能为杂质;
C、①④组合中氮气的氧元素的质量分数为0,小于57%;故可能为杂质;
D、②④组合中二者的氧元素质量分数都小于57%,故可能为杂质;
故选B
点评:本题主要考查了元素质量分数的计算,元素的质量分数=
 ×100%.
×100%. 
练习册系列答案
 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案
相关题目
