题目内容
8.化学是一门以实验为基础的学科.根据图1,回答问题.
(1)a仪器的名称为长颈漏斗.
(2)实验室用A装置制O2的化学方程式为2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑,选用的收集装置是C(填字母序号).查阅资料后可知,锰酸钾可溶于水,若要从高锰酸钾完全分解后的固体残渣中回收二氧化锰,正确操作的顺序是bcda(填写选项序号).
a.烘干 b.溶解 c.过滤 d.洗涤
(3)制取CO2用装置F替代装置B的优点是可以控制反应的发生和停止.通过装置B、E来验证二氧化碳的性质,实验过程中观察到E中有气泡冒出,但澄清的石灰水未变浑浊,试分析其可能的原因二氧化碳中混有氯化氢气体.
(4)氨气是一种无色、有刺激性气味的气体,密度比空气小,极易溶于水.实验室用加热氯化铵和氢氧化钙的固体混合物制取氨气,其发生装置(图2),可选用A(填装置编号),收集氨气时最好选用下列装置中的G装置与②装置相连接(填数字编号).
分析 长颈漏斗方便加液体药品,制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.查阅资料后可知,锰酸钾可溶于水,若要从高锰酸钾完全分解后的固体残渣中回收二氧化锰,正确操作的顺序是:溶解、过滤、洗涤、干燥;实验室用加热氯化铵和氢氧化钙的固体混合物制取氨气,因此需要加热;收集氨气时最好选用下列装置中的G装置与②装置相连接,防止氨气污染空气.
解答 解:(1)长颈漏斗方便加液体药品,故答案为:长颈漏斗;
(2)氯酸钾在二氧化锰做催化剂和加热的条件下生成氯化钾和氧气,配平即可;氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集;查阅资料后可知,锰酸钾可溶于水,若要从高锰酸钾完全分解后的固体残渣中回收二氧化锰,正确操作的顺序是:溶解、过滤、洗涤、干燥;故答案为:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;C;bcda;
(3)制取CO2用装置F替代装置B的优点是:可以控制反应的发生和停止;通过装置B、E来验证二氧化碳的性质,实验过程中观察到E中有气泡冒出,但澄清的石灰水未变浑浊,试分析其可能的原因:二氧化碳中混有氯化氢气体;故答案为:可以控制反应的发生和停止;二氧化碳中混有氯化氢气体;
(4)实验室用加热氯化铵和氢氧化钙的固体混合物制取氨气,因此需要加热;收集氨气时最好选用下列装置中的G装置与②装置相连接,防止氨气污染空气;故答案为:A;②;
点评 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写、物质的分离等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案| A. | 非金属元素:Be、Br、B | B. | 碱:烧碱、熟石灰、纯碱 | ||
| C. | 混合物:钢、软水、水银 | D. | 有机物:CH3COOH、CO(NH2)2、C6H12O6 |
| A. | 验证碱能与酸反应:将H2SO4溶液滴入Cu(OH)2中 | |
| B. | 检验氧气是否集满:将带火星木条伸到集气瓶口,观察是否木条是否复燃 | |
| C. | 验证质量守恒定律:敞口试管中将锌粒与稀硫酸混合,比较混合前后溶液的质量 | |
| D. | 鉴别H2、CH4、CO三种气体:分别将燃着的木条伸入集气瓶内,观察现象 |
| A. | S2--硫离子 | B. | 3O-3个氧元素 | C. | Fe2O3-氧化铁 | D. | 2H2-2个氢气分子 |
| A. | 用加热方法给聚乙烯塑料袋封口 | |
| B. | 用酒精浸泡捣烂的某些植物花瓣可制酸碱指示剂 | |
| C. | 用2B铅笔芯做导电性实验 | |
| D. | 用淬火处理后的缝衣钢针制钓鱼钩 |

| A. | 该物质的化学式为C8H8O3 | |
| B. | 该物质分子中氢、氧原子的个数比为8:3 | |
| C. | 该物质完全燃烧生成二氧化碳和水 | |
| D. | 该物质中含氧元素的质量分数最小 |
| A. | 将光亮的铁丝由瓶口慢慢插入盛有氧气的集气瓶中 | |
| B. | 将铁丝绕成螺旋状可以增大铁丝的受热面积,还便于聚热,防止热量散失 | |
| C. | 待铁丝下端的火柴即将燃尽时将铁丝插入集气瓶中 | |
| D. | 该实验标志新物质生成的现象是生成了黑色的四氧化三铁 |
(1)认识金属元素存在:自然界中大多数金属都以化合物的形式存在.下列矿石的主要成分属于氧化物的是AD(填字母序号,下同);
A.铝土矿 (主要成分A1203) B.辉铜矿(主要成分Cu2S)
C.菱铁矿 (主要成分FeC03) D.磁铁矿 (主要成分Fe304)
(2)探究金属物理性质:
如表是A、B、C三种金属的部分物理性质.
| 性质 金属 | 导电性(100为标准) | 密度(g/cm3) | 熔点(℃) | 硬度(10为标准) |
| A | 99 | 8.92 | 1083 | 3 |
| B | 61 | 2.70 | 660 | 2.9 |
| C | 17 | 7.86 | 1535 | 5 |
②C的合金通常可以做菜刀、锤子等,其合金的硬度>5(填“>”“<”或“=”).
(3)探究金属化学性质:金属原子容易失去最外层电子,化学性质活泼.
材料:我国第四套人民币中的一元硬币是钢芯镀镍(Ni),镍与稀硫酸能发生下列反应:
Ni+H2SO4═NiSO4+H2↑.
写出Ni与CuSO4溶液发生置换反应的方程式Ni+CuSO4═Cu+NiSO4.
(4 )认识金属的制备:工业上常采用还原法、置换法、电解法制备金属.
用一氧化碳还原赤铁矿冶铁反应的化学方程式为_Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2 .
(5)金属在生产生活中应用广泛.如图,向一定量硝酸银溶液中加入铜和锌的混合粉末,充分反应后过滤,得溶液甲和固体乙.
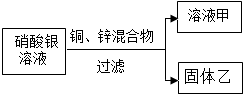
①若乙中含有锌、铜、银三种固体,此时向固体乙中加入稀盐酸,发生反应的化学方程式为Zn+2HCl=ZnCl2+H2↑.
②若溶液甲显蓝色,是因为Cu+2AgNO3═2Ag+Cu(NO3)2(用化学反应方程式表示),此时固体乙中一定含有的物质是银.