题目内容
17.下列事实中,能用质量守恒定律解释的是( )| A. | 煤炭燃烧后,质量减少 | |
| B. | “卫生球”放在衣柜里,质量减少 | |
| C. | 50毫升酒精和50毫升水混合后总体积小于100毫升 | |
| D. | 衣服被雨水淋湿后,质量增加 |
分析 质量守恒定律是物质在发生化学变化中表现出来的一种规律,适用于化学变化;物质发生物理变化,则不适用于质量守恒定律来解释;据此进行分析判断.
解答 解:A、煤炭燃烧,属于化学变化,能用质量守恒定律解释;故选项正确.
B、“卫生球”放在衣柜里,质量减少属于升华现象,没有新物质生成,属于物理变化,不能用质量守恒定律解释,故选项错误.
C、酒精与水混合后体积变小,是因为分子间有间隔,没有新物质生成,属于物理变化,不能用质量守恒定律解释,故选项错误.
D、衣服被雨水淋湿,没有新物质生成,属于物理变化,不能用质量守恒定律解释,故选项错误.
故选:A.
点评 质量守恒定律是物质在发生化学变化中表现出来的一种规律,适用于化学变化,掌握化学变化和物理变化的判别是解题的关键.

练习册系列答案
 智能训练练测考系列答案
智能训练练测考系列答案
相关题目
3.某同学用pH试纸测出日常生活中几种常见物质的pH,其中酸性最强的是( )
| A. | 肥皂水:pH=10 | B. | 酸奶:pH=4 | C. | 漂白液:pH=13 | D. | 洁厕精:pH=1 |
8.某化学兴趣小组为了探究铬与常见金属铝、铜在金属活动性顺序的相对位置关系,进行了如下探究活动:
【查阅资料】铬(Cr)是银白色有光泽的金属,在空气中表面能生成抗腐蚀的致密氧化膜.铬能与稀硫酸反应,生成氢气和硫酸铬(CrSO4).
【提出猜想】对这三种金属的活动性顺序提出了如下猜想:
猜想①:Cr>Al>Cu
猜想②:Cr>Cu>Al
猜想③:Al>Cr>Cu
猜想④:Al>Cu>Cr
【讨论交流】根据已学的金属活动性顺序和已查阅的资料分析,肯定不能成立的是猜想②④(填序号).
【实验设计及过程】请将表中的内容填写完整.
【实验反思】
(1)将金属片投入稀硫酸前应先打磨金属片的目的是除去金属表面氧化物,有利于直接反应.
(2)有同学提出探究金属活动性强弱还可以依据“金属与金属化合物溶液是否发生置换反应”来判断.为了验证甲、乙、丙三种金属的活动性依次减弱,某同学设计了如下方案:
①把甲放入乙的化合物溶液中;
②把乙放入丙的化合物溶液中;
③把甲放入丙的化合物溶液中;
你认为上述方案中的③(填序号)没有必要做.
【查阅资料】铬(Cr)是银白色有光泽的金属,在空气中表面能生成抗腐蚀的致密氧化膜.铬能与稀硫酸反应,生成氢气和硫酸铬(CrSO4).
【提出猜想】对这三种金属的活动性顺序提出了如下猜想:
猜想①:Cr>Al>Cu
猜想②:Cr>Cu>Al
猜想③:Al>Cr>Cu
猜想④:Al>Cu>Cr
【讨论交流】根据已学的金属活动性顺序和已查阅的资料分析,肯定不能成立的是猜想②④(填序号).
【实验设计及过程】请将表中的内容填写完整.
| 实验操作 | 实验现象 | 实验结论 |
| 室温下,将大小相同并打磨光亮的铬片、铝片、铜片分别浸入盛有体积相同、溶质质量分数相同的稀硫酸试管中 | 铬片表面产生气泡缓慢,铝片表面产生气泡较快,铜片表面无现象 | 猜想③(填序号)成立 |
(1)将金属片投入稀硫酸前应先打磨金属片的目的是除去金属表面氧化物,有利于直接反应.
(2)有同学提出探究金属活动性强弱还可以依据“金属与金属化合物溶液是否发生置换反应”来判断.为了验证甲、乙、丙三种金属的活动性依次减弱,某同学设计了如下方案:
①把甲放入乙的化合物溶液中;
②把乙放入丙的化合物溶液中;
③把甲放入丙的化合物溶液中;
你认为上述方案中的③(填序号)没有必要做.
5.高铁酸钠(Na2FeO4)是一种新型高效的水处理剂.下列有关高铁酸钠的说法正确的是( )
| A. | 属于混合物 | B. | 属于氧化物 | ||
| C. | 钠、铁、氧三种元素质量比是2:1:4 | D. | 铁元素化合价为+6 |
6.过氧化钠(Na2O2)是一种淡黄色粉末,可作为潜水艇或呼吸面具有供氧剂.人呼出气体的主要成份有氮气、氧气、二氧化碳和水蒸气,二氧化碳和水能分别与Na2O2反应生成氧气.为了探究Na2O2在潜水艇中反应后的物质,明明同学设计了如图1所示模拟实验.
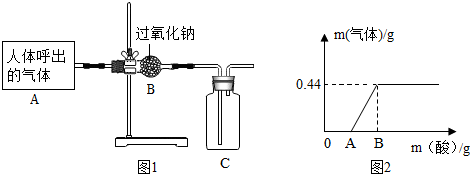
【猜想与假设】
(1)明明猜想生成的固体物质是:(Ⅰ)氢氧化钠(Ⅱ)碳酸钠(Ⅲ)氢氧化钠和碳酸钠
【实验与验证】
(2)明明通过以下实验探究来验证他的猜想:
实验①:取少量反应后干燥管中的固体样品,置于试管中,向其中加入稀盐酸,发现有气泡产生,该气体通入澄清石灰水,石灰水变浑浊,证明猜想(Ⅰ)不成立.
实验②:取少量反应后干燥管中的固体样品,置于试管中,加水溶解,配成溶液,再用洁净干燥的玻璃棒蘸取该溶液滴到湿润的pH试纸上,测得pH=10,证明猜想(Ⅱ)不成立.对他的操作方法、测量结果及结论的评价,正确的是C.
A.方法正确,结果正确,且结论正确 B.方法不正确,结果偏大,但结论正确
C.方法不正确,结果偏小,结论不正确 D.方法正确,结果正确,但结论不正确
实验③:继续探究,请将明明的探究过程填写完整.
于是明明得出结论:猜想(Ⅱ)不成立,猜想(Ⅲ)成立.该样品中含氢氧化钠的原因(用化学方程式表示)2NaOH+CO2=Na2CO3+H2O.
【反思与评价】
(3)明明认为碳酸钠一定是Na2O2与呼出气体中的二氧化碳反应生成的,因为过氧化钠和二氧化碳反应生成碳酸钠和氧气;他认为也可在上述实验装置中的A、B之间增加一个装有浓硫酸的干燥装置,重复实验①即可证明自己的判断.
【拓展与延伸】
(4)明明另取少量反应后干燥管中的固体样品,配制成溶液,向其中逐滴滴加稀盐酸,产生气体的质量与加入稀盐酸的质量的关系如图2所示.
①开始滴加盐酸时没有产生气体的原因是盐酸与氢氧化钠发生了反应.
②计算该样品中碳酸钠的质量;
③若A为10克,B为20克,则所用稀盐酸的溶质的质量分数为多少?

【猜想与假设】
(1)明明猜想生成的固体物质是:(Ⅰ)氢氧化钠(Ⅱ)碳酸钠(Ⅲ)氢氧化钠和碳酸钠
【实验与验证】
(2)明明通过以下实验探究来验证他的猜想:
实验①:取少量反应后干燥管中的固体样品,置于试管中,向其中加入稀盐酸,发现有气泡产生,该气体通入澄清石灰水,石灰水变浑浊,证明猜想(Ⅰ)不成立.
实验②:取少量反应后干燥管中的固体样品,置于试管中,加水溶解,配成溶液,再用洁净干燥的玻璃棒蘸取该溶液滴到湿润的pH试纸上,测得pH=10,证明猜想(Ⅱ)不成立.对他的操作方法、测量结果及结论的评价,正确的是C.
A.方法正确,结果正确,且结论正确 B.方法不正确,结果偏大,但结论正确
C.方法不正确,结果偏小,结论不正确 D.方法正确,结果正确,但结论不正确
实验③:继续探究,请将明明的探究过程填写完整.
| 实验操作 | 现象或测定结果 | 结论 |
| 步骤1:取少量反应后干燥管中的固体样品溶于水配成溶液,滴加过量的氯化钙溶液,充分反应后过滤 | 有白色沉淀生成 | 该样品中有碳酸钠 |
| 步骤2:用PH试纸测定步骤1所得滤液的酸碱度. | pH>7 | 该样品中含有氢氧化钠 |
【反思与评价】
(3)明明认为碳酸钠一定是Na2O2与呼出气体中的二氧化碳反应生成的,因为过氧化钠和二氧化碳反应生成碳酸钠和氧气;他认为也可在上述实验装置中的A、B之间增加一个装有浓硫酸的干燥装置,重复实验①即可证明自己的判断.
【拓展与延伸】
(4)明明另取少量反应后干燥管中的固体样品,配制成溶液,向其中逐滴滴加稀盐酸,产生气体的质量与加入稀盐酸的质量的关系如图2所示.
①开始滴加盐酸时没有产生气体的原因是盐酸与氢氧化钠发生了反应.
②计算该样品中碳酸钠的质量;
③若A为10克,B为20克,则所用稀盐酸的溶质的质量分数为多少?
7.下列除去杂质(括号内为杂质)的方法正确的是( )
| A. | CO(CO2):通过灼热的氧化铜 | B. | MgSO4 (CuSO4):加入适量的氢氧化镁 | ||
| C. | KNO3溶液(NaCl):降温结晶 | D. | 铁粉(氧化铜粉末):加入足量稀硫酸 |
