题目内容
某同学对某地工业废水(含有硫酸和盐酸)中的H2SO4 进行测定.取50g该废水于烧杯中,加入足量的BaCl2溶液,充分反应中,过滤、洗涤、干燥得到BaSO4固体11.65g.通过计算回答下列问题:
(1)50g该废水中H2SO4 的质量
(2)若改用KOH溶液来测定50g该废水中H2SO4 的含量,结果会 (填“偏高”、“偏低”、“不变”),理由是 .
【答案】
(1)50g该废水中H2SO4 的质量为4.9g.(2)偏高;废水中含有盐酸,盐酸也会消耗氢氧化钾.
【解析】
试题分析:1)设50g废水中硫酸的质量为x.
H2SO4+BaCl2=BaSO4↓+2HCl
98 233
x 11.65g
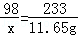
x=4.9g
(2)由于废水中除含硫酸外还含有盐酸,盐酸也能中和氢氧化钾,使消耗的氢氧化钾会增大,再由消耗的氢氧化钾的质量计算出的硫酸的质量会比废水中硫酸的质量大(其实就是因为盐酸消耗的氢氧化钾也被当成硫酸消耗的,所以导致硫酸的含量偏高).
考点:根据化学反应方程式的计算.

练习册系列答案
 字词句段篇系列答案
字词句段篇系列答案
相关题目