题目内容
某工业碳酸钠样品中混有少量氯化钠,为了测定样品的纯度,向12.0g样品中滴加稀盐酸至恰好完全反应,待二氧化碳气体不再放出后,去除溶液中的水分,最终得到13.1g氯化钠固体。试计算工业碳酸钠样品中Na2CO3的质量分数。(结果精确到0.1%)
【解】设:12g样品中含Na2CO3的质量为x,反应生成氯化钠的 质量为y。
质量为y。
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 117
x y
106 /x = 117 /y
y = 117x / 106
所得固体氯化钠的质量:12g-x+117x/106=13.1g
x=10.6g
该样品中含Na2CO3的质量分数为: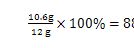
答:工业碳酸钠样品中Na2CO3的质量分数是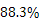 。
。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
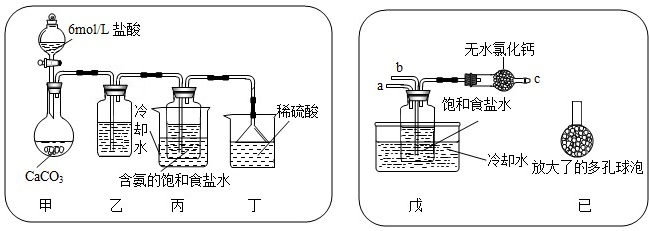
 (2010?大连二模)为测定某工业纯碱中碳酸纳(含少量氯化钠)的质量分数,某活动小组同学采用气体法:通过测定碳酸钠与酸反应产生的二氧化碳的质量来推算碳酸纳的质量.他们设计以下实验方案并实施(装置气密性良好,操作规范、计算无误):
(2010?大连二模)为测定某工业纯碱中碳酸纳(含少量氯化钠)的质量分数,某活动小组同学采用气体法:通过测定碳酸钠与酸反应产生的二氧化碳的质量来推算碳酸纳的质量.他们设计以下实验方案并实施(装置气密性良好,操作规范、计算无误):