题目内容
某化学兴趣小组的同学对实验室制取氧气的实验展开了如下探究:(1)小明同学选用如图1所示的装置制取氧气.制取过程中所发生反应的化学反应方程式为:______ 2H2O+O2↑
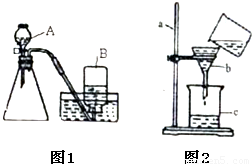
【答案】分析:制取装置包括加热和不需加热两种,如果用双氧水制氧气就不需要加热,过氧化氢在二氧化锰做催化剂的条件下生成水和氧气,观察导气管口是否有连续的气泡出现,该实验操作的目的是:检查装置的气密性;氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.由表格数据可知:上述实验应测量的“待测数据”是得到相同质量的氧气所需要的时间;若实验②比实验①的“待测数据”更小,说明氧化铜能加快氯酸钾的分解速率;将实验②反应后的固体经提纯分离仍得到0.5克黑色粉末,再将黑色粉末放入试管中,加入氯酸钾固体加热,一会儿就有气泡冒出,说明氧化铜还能作氯酸钾的催化剂;设计实验③和实验②对比的目的是:比较氧化铜和二氧化锰哪个催化效果更好.根据表格数据分析过氧化氢溶液的浓度对反应速度有怎样的影响:过氧化氢溶液的浓度越大,反应的速度越快;二氧化锰不溶于水,因此采用过滤、洗涤、干燥、称量,她用如图2所示的装置进行实验,图中的三处错误是:用烧杯直接向漏斗内倒液体;液面高于滤纸边缘;漏斗的下端在烧杯的中央.
解答:解:(1)如果用双氧水制氧气就不需要加热,过氧化氢在二氧化锰做催化剂的条件下生成水和氧气;观察导气管口是否有连续的气泡出现,该实验操作的目的是:检查装置的气密性;故答案为:2H2O2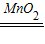 2H2O+O2↑;检查装置的气密性;
2H2O+O2↑;检查装置的气密性;
(2)由表格数据可知:上述实验应测量的“待测数据”是得到相同质量的氧气所需要的时间;若实验②比实验①的“待测数据”更小,说明氧化铜能加快氯酸钾的分解速率;将实验②反应后的固体经提纯分离仍得到0.5克黑色粉末,再将黑色粉末放入试管中,加入氯酸钾固体加热,一会儿就有气泡冒出,说明氧化铜还能作氯酸钾的催化剂;设计实验③和实验②对比的目的是:比较氧化铜和二氧化锰哪个催化效果更好;故答案为:①得到相同质量的氧气所需要的时间;②小;③加入氯酸钾固体加热,一会儿就有气泡冒出;比较氧化铜和二氧化锰哪个催化效果更好;
(3)根据表格数据分析过氧化氢溶液的浓度对反应速度有怎样的影响:过氧化氢溶液的浓度越大,反应的速度越快;二氧化锰不溶于水,因此采用过滤、洗涤、干燥、称量,她用如图2所示的装置进行实验,图中的三处错误是:用烧杯直接向漏斗内倒液体;液面高于滤纸边缘;漏斗的下端在烧杯的中央;故答案为:①过氧化氢溶液的浓度越大,反应的速度越快;②过滤;用烧杯直接向漏斗内倒液体;液面高于滤纸边缘;漏斗的下端在烧杯的中央
点评:本考点主要考查气体的制取装置和收集装置的选择、影响化学反应速度的因素,同时也考查了化学方程式的书写和混合物的分离方法等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.
解答:解:(1)如果用双氧水制氧气就不需要加热,过氧化氢在二氧化锰做催化剂的条件下生成水和氧气;观察导气管口是否有连续的气泡出现,该实验操作的目的是:检查装置的气密性;故答案为:2H2O2
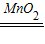 2H2O+O2↑;检查装置的气密性;
2H2O+O2↑;检查装置的气密性;(2)由表格数据可知:上述实验应测量的“待测数据”是得到相同质量的氧气所需要的时间;若实验②比实验①的“待测数据”更小,说明氧化铜能加快氯酸钾的分解速率;将实验②反应后的固体经提纯分离仍得到0.5克黑色粉末,再将黑色粉末放入试管中,加入氯酸钾固体加热,一会儿就有气泡冒出,说明氧化铜还能作氯酸钾的催化剂;设计实验③和实验②对比的目的是:比较氧化铜和二氧化锰哪个催化效果更好;故答案为:①得到相同质量的氧气所需要的时间;②小;③加入氯酸钾固体加热,一会儿就有气泡冒出;比较氧化铜和二氧化锰哪个催化效果更好;
(3)根据表格数据分析过氧化氢溶液的浓度对反应速度有怎样的影响:过氧化氢溶液的浓度越大,反应的速度越快;二氧化锰不溶于水,因此采用过滤、洗涤、干燥、称量,她用如图2所示的装置进行实验,图中的三处错误是:用烧杯直接向漏斗内倒液体;液面高于滤纸边缘;漏斗的下端在烧杯的中央;故答案为:①过氧化氢溶液的浓度越大,反应的速度越快;②过滤;用烧杯直接向漏斗内倒液体;液面高于滤纸边缘;漏斗的下端在烧杯的中央
点评:本考点主要考查气体的制取装置和收集装置的选择、影响化学反应速度的因素,同时也考查了化学方程式的书写和混合物的分离方法等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

练习册系列答案
 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案
相关题目
 12、碳酸氢钠(NaHCO3)俗称小苏打,常用于食品和医药工业.某化学兴趣小组的同学对碳酸氢钠的性质进行探究.
12、碳酸氢钠(NaHCO3)俗称小苏打,常用于食品和医药工业.某化学兴趣小组的同学对碳酸氢钠的性质进行探究.


 (2012?烟台)某化学兴趣小组的同学用如图所示装置进行实验(装置气密性良好),先关闭止水夹,将足量的氢氧化钠溶液滴入烧瓶中,充分吸收掉二氧化碳后,再打开止水夹.
(2012?烟台)某化学兴趣小组的同学用如图所示装置进行实验(装置气密性良好),先关闭止水夹,将足量的氢氧化钠溶液滴入烧瓶中,充分吸收掉二氧化碳后,再打开止水夹. 某化学兴趣小组的同学在实验室配制质量分数为8%的氢氧化钠溶液,并用其测定某稀盐酸中溶质的质量分数.
某化学兴趣小组的同学在实验室配制质量分数为8%的氢氧化钠溶液,并用其测定某稀盐酸中溶质的质量分数.