题目内容
14.在世界范围内,据统计化肥对粮食增产的贡献率已超过40%,如图是两种氨肥标签的一部分.请根据图示中的信息回答下列问题.
(1)从标签上看,碳酸氢铵不同于尿素的化学性质是B(填字母序号);
A.易溶于水 B.受热易分解 C.有挥发性
(2)碳酸氢铵的相对分子质量为79;
(3)计算纯尿素中氮元素的质量分数.这种尿素肥料的纯度至少是多少?(计算结果精确至0.1%)
分析 (1)根据标签的内容即可获得物质的性质;
(2)根据相对分子的质量为组成分子的各原子的相对原子质量之和,进行分析解答.
(3)根据元素的质量分数公式计算出尿素中氮元素的质量分数,然后根据“46%÷尿素中氮元素的质量分数”计算即可.
解答 解:(1)根据标签可以看出,这两种物质保存时都需要防潮,因此都是易溶于水的物质,碳酸氢铵要避免高温施用,说明碳酸氢铵受热易分解;故填:B;
(2)根据相对分子的质量为组成分子的各原子的相对原子质量之和,碳酸氢铵的相对分子质量为14+1×4+1+12+16×3=79.故填:79;
(3)尿素中氮元素的质量分数为$\frac{14×2}{12+16+(14+1×2)×2}×100%$≈46.7%;这种尿素肥料的纯度至少是42.3%÷46.7%≈90.6%.故填:90.6%.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案 品学双优卷系列答案
品学双优卷系列答案 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案
相关题目
9.下列说法正确的是( )
| A. | 向氯化钙溶液中通入二氧化碳气体会产生白色沉淀 | |
| B. | 向硫酸铜溶液中加入金属钠会析出红色固体 | |
| C. | 向氯化铜溶液中滴加某溶液产生蓝色沉淀,则所加溶液一定为碱溶液 | |
| D. | 向室温下饱和的石灰水中加入少量氧化钙固体,其溶解度先变小后变大 |
19.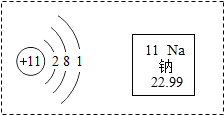 元素周期表是学习和研究化学的重要工具.请根据下表(元素周期表的部分内容)回答有关问题:
元素周期表是学习和研究化学的重要工具.请根据下表(元素周期表的部分内容)回答有关问题:
(1)请从上表中查出关于硼元素的一条信息:它是的质子数是5或它的相对原子质量为10.81等.
(2)不同元素的本质区别是A
A.质子数 B.电子数 C.中子数 D.相对原子质量
(3)如图是钠原子的结构示意图,判断该原子容易失去(填“得到”或“失去”)电子,钠离子的符号为Na+.
(4)在元素周期表中,同一族(纵行)的元素具有相似的化学性质.则下列各组元素具有相似化学性质的是b、d(填标号).
A.C和Ne B.Be和Mg C.Al和Si D.F和Cl
(5)第9号氟元素和氢元素形成的化合物的水溶液氢氟酸(HF),可用于玻璃雕刻,其主要原理是氢氟酸与玻璃的主要成分二氧化硅(SiO2)发生反应,生成四氟化硅气体(SiF4)和水(H2O),用化学式表示该反应4HF+SiO2=SiF4+2H2O.
 元素周期表是学习和研究化学的重要工具.请根据下表(元素周期表的部分内容)回答有关问题:
元素周期表是学习和研究化学的重要工具.请根据下表(元素周期表的部分内容)回答有关问题:| 族 周期 | I A | II A | IIIA | IVA | VA | VIA | VIIA | 0 |
| 3 | 3 Li 锂 6.941 | 4 Be 铍 9.012 | 5 B 硼 10.81 | 6 C 碳 12.01 | 7 N 氮 14.01 | 8 O 氧 16.00 | 9 F 氟 19.00 | 10 Ne 氖 20.18 |
| 3 | 11 Na 钠 22.99 | 12 Mg 镁 24.31 | 13 Al 铝 26.98 | 14 Si 硅 28.09 | 15 P 磷 30.97 | 16 S 硫 32.06 | 17 Cl 氯 35.45 | 18 Ar 氩 39.95 |
(2)不同元素的本质区别是A
A.质子数 B.电子数 C.中子数 D.相对原子质量
(3)如图是钠原子的结构示意图,判断该原子容易失去(填“得到”或“失去”)电子,钠离子的符号为Na+.
(4)在元素周期表中,同一族(纵行)的元素具有相似的化学性质.则下列各组元素具有相似化学性质的是b、d(填标号).
A.C和Ne B.Be和Mg C.Al和Si D.F和Cl
(5)第9号氟元素和氢元素形成的化合物的水溶液氢氟酸(HF),可用于玻璃雕刻,其主要原理是氢氟酸与玻璃的主要成分二氧化硅(SiO2)发生反应,生成四氟化硅气体(SiF4)和水(H2O),用化学式表示该反应4HF+SiO2=SiF4+2H2O.
6.继食盐加碘工程之后,我国又启动酱油加碘工程.这里的继食盐加碘工程之后,我国又启动酱油加碘工程.( )
| A. | 铁单质 | B. | 铁元素 | ||
| C. | 铁原子 | D. | 铁的相对原子质量 |
4.硫在氧气中燃烧,最能说明了该变化是化学变化的是( )
| A. | 比空气中燃烧更旺 | B. | 生成刺激性气味的气体 | ||
| C. | 放出大量的热 | D. | 发出明亮的蓝紫色火焰 |
 如图是某人画的实验室的过滤装置图.
如图是某人画的实验室的过滤装置图.