题目内容
碳在空气中燃烧有两个反应,一定条件下,12g碳与20g氧气完全反应,求生成物.
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:根据化学方程式,12g碳在氧气中充分燃烧生成二氧化碳时需要32g氧气,故该题中氧气不足,碳有剩余,会与生成的二氧化碳反应生成一氧化碳,故生成物为一氧化碳和二氧化碳的混合气体,据此分析.
解答:解:设20g氧气反应碳的质量为x,生成二氧化碳的质量为y
C+O2
CO2
12 32 44
x 20g y
=
=
解得:x=7.5g y=27.5g
则剩余碳的质量为:12g-7.5g=4.5g
设4.5g碳反应消耗二氧化碳的质量为m,生成一氧化碳的质量为n
C+CO2
2CO
12 44 56
4.5g m n
=
=
解得:m=16.5g,n=21g
故所得气体为一氧化碳和二氧化碳的混合气体,二氧化碳的质量为:27.5g-16.5g=11g,一氧化碳为21g.
答:生成物为一氧化碳和二氧化碳的混合气体,二氧化碳的质量为11g,一氧化碳为21g.
C+O2
| ||
12 32 44
x 20g y
| 12 |
| 32 |
| x |
| 20g |
| 32 |
| 44 |
| 20g |
| y |
解得:x=7.5g y=27.5g
则剩余碳的质量为:12g-7.5g=4.5g
设4.5g碳反应消耗二氧化碳的质量为m,生成一氧化碳的质量为n
C+CO2
| ||
12 44 56
4.5g m n
| 12 |
| 44 |
| 4.5g |
| m |
| 12 |
| 56 |
| 4.5g |
| n |
解得:m=16.5g,n=21g
故所得气体为一氧化碳和二氧化碳的混合气体,二氧化碳的质量为:27.5g-16.5g=11g,一氧化碳为21g.
答:生成物为一氧化碳和二氧化碳的混合气体,二氧化碳的质量为11g,一氧化碳为21g.
点评:本题主要考查碳在氧气中不完全燃烧时的情况,要仔细分析.

练习册系列答案
 小学教材全测系列答案
小学教材全测系列答案 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案
相关题目
鉴别H2、O2、CO2、空气四种气体的最简便的方法是( )
| A、试验四种气体的溶解性 |
| B、用燃着的木条检验 |
| C、向瓶内倒入澄清石灰水 |
| D、测定四种气体的密度 |
下列有关“化学实验”的说法正确的是( )
| A、木炭在空气中燃烧发出微弱的红光,在氧气中燃烧发出明亮的火焰 |
| B、在加热高锰酸钾制取氧气时,装置漏气会造成收集到的氧气不纯 |
| C、在过滤操作中,滤纸紧贴漏斗壁是为了使过滤更快 |
| D、在实验中,如果没有说明用量,固体一般按最少量取1~2g |
下列物质的用途主要由化学性质决定的是( )
| A、干冰用作人工降雨剂 |
| B、富氧炼钢 |
| C、活性炭除去冰箱中的异味 |
| D、金刚石切割玻璃 |
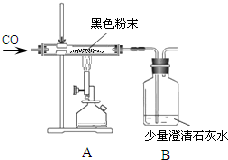 小新同学为确定某份黑色粉末,称取该粉末8.0g装入硬质玻璃管中,按如图在通风橱中进行实验.开始时缓缓通入CO气体,过一段时间后再加热使其充分反应.待反应完全后,停止加热,仍继续通CO气体直至玻璃管冷却.反应前后称量相关装置和物质的总质量,其数据如下表:
小新同学为确定某份黑色粉末,称取该粉末8.0g装入硬质玻璃管中,按如图在通风橱中进行实验.开始时缓缓通入CO气体,过一段时间后再加热使其充分反应.待反应完全后,停止加热,仍继续通CO气体直至玻璃管冷却.反应前后称量相关装置和物质的总质量,其数据如下表: