题目内容
【题目】硫酸亚铁可用于治疗缺铁性贫血,其中铁元素的化合价为 , 计算:
【答案】+2
(1)硫酸亚铁(FeSO4)的相对分子质量= , 其中铁元素的质量分数为;
(2)某贫血患者共需补充1.4g铁元素,服用的药物中需含硫酸亚铁克?
【答案】
(1)152;36.8%
(2)3.8g
【解析】解:根据在化合物中正负化合价代数和为零,硫酸根显﹣2,设铁元素的化合价是x,则:x+(﹣2)=0,则x=+2.(1)硫酸亚铁的相对分子质量为56+32+16×4=152.(2)硫酸亚铁中铁元素的质量分数 ![]() ×100%≈36.8%.(3)某贫血患者需补充1.4g铁,至少需要服用硫酸亚铁的质量为:1.4g÷36.8%=3.8g.
×100%≈36.8%.(3)某贫血患者需补充1.4g铁,至少需要服用硫酸亚铁的质量为:1.4g÷36.8%=3.8g.
所以答案是:+2;(1)152;(2)36.8%;(43)3.8g.

练习册系列答案
相关题目
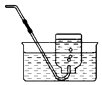
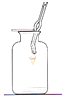
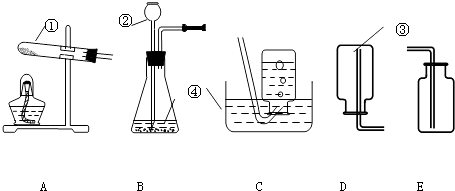
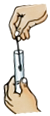
【题目】对下列实验指定容器中的水,其解释没有体现水的主要作用的是( )
实 |
|
|
|
|
解释 | 集气瓶中的水:吸收放出的热量 | 集气瓶中的水:水将集气瓶内的空气排干净,便于观察氧气何时收集满 | 量筒中的水:通过水体积的变化得出氧气体积 | 集气瓶中的水:冷却溅落熔化物,防止集气瓶炸裂 |
A | B | C | D |
A.A
B.B
C.C
D.D