题目内容
16.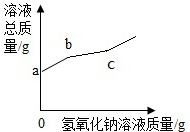 向一含有盐酸的氯化铁溶液边震荡边逐滴滴入氢氧化钠溶液,直至过量,某同学画了如图,要表明反应过程中,溶液总质量与滴入氢氧化钠溶液质量的关系.
向一含有盐酸的氯化铁溶液边震荡边逐滴滴入氢氧化钠溶液,直至过量,某同学画了如图,要表明反应过程中,溶液总质量与滴入氢氧化钠溶液质量的关系.请看图分析:
(1)b点对应的溶液中,溶质化学式为NaCl、FeCl3
(2)写出先后发生反应的化学方程式:(1)HCl+NaOH=NaCl+H2O,(2)FeCl3+3NaOH=Fe(OH)3↓+3NaCl.
分析 根据物质的性质进行分析,在盐酸和氯化铁的溶液中滴入氢氧化钠溶液,氢氧化钠首先与盐酸反应,故开始溶液质量增加,当盐酸完全反应以后,氢氧化钠与氯化铁反应生成氢氧化铁沉淀,根据加入的氢氧化钠的质量与生成的氢氧化铁质量差判断溶液质量的变化,据此解答即可.
解答 解:(1)盐酸和氯化铁的混合溶液中,加入氢氧化钠溶液,氢氧化钠首先与盐酸反应生成氯化钠和水,当b点时,出现拐点,说明此时盐酸全部参加反应,则溶液中的溶质有生成的氯化钠和没参加反应的氯化铁,故填:NaCl、FeCl3;
(2)盐酸和氯化铁的混合溶液中,加入氢氧化钠溶液,氢氧化钠首先与盐酸反应生成氯化钠和水,故开始时溶液质量在增加;当盐酸消耗尽,氢氧化钠和氯化铁反应生成氢氧化铁沉淀和氯化钠,故反应的化学方程式分别为:HCl+NaOH=NaCl+H2O,FeCl3+3NaOH=Fe(OH)3↓+3NaCl.
故答案为:
(1)NaCl、FeCl3;(2)HCl+NaOH=NaCl+H2O,FeCl3+3NaOH=Fe(OH)3↓+3NaCl.
点评 本题考查了常见酸碱以及盐之间的反应,完成此题,可以依据已有的知识进行.

练习册系列答案
 课课练江苏系列答案
课课练江苏系列答案 名牌中学课时作业系列答案
名牌中学课时作业系列答案
相关题目
20.化学变化中常伴随一些颜色的变化,以下溶液或沉淀是蓝色的是( )
| A. | FeCl2 | B. | FeCl3 | C. | Cu(OH)2 | D. | NaCl |
11.下列化学方程式正确的是( )
| A. | BaCl2+Mg(NO3)2═Ba(NO3)2↓+MgCl2 | B. | Na2SO4+BaCO3═BaSO4↓+Na2CO3 | ||
| C. | Mg+2AgCl═MgCl2+2Ag | D. | 2Al+3CuCl2═2AlCl3+3Cu |
1.谢老师交给某研究性学习小组一个任务:测定实验室里一瓶久置的NaOH固体是否变质.该小组的同学进行了如下实验探究:
【提出问题】猜想I:没变质,全部是NaOH;猜想II:部分变质,既含有NaOH,又含有Na2CO3:猜想Ⅲ:完全变质,全部是Na2CO3.
【查阅资料】①已知反应:BaCl2+Na2CO3=2NaCl+BaCO3↓
②部分盐溶液在常温下的pH如下:
【设计方案并进行实验】
请你与他们一起共同完成,并回答所给问题.
(3)上述步骤①中,所用称量仪器的名称是托盘天平
(4)滴加过量BaCl2溶液的目的是检验并除去碳酸钠
(5)【实验结论】通过实验,说明上述猜想Ⅱ是正确的.
| 盐溶液 | NaCl | Na2CO3 | BaCl2 |
| pH | 等于7 | 大于7 | 等于7 |
【查阅资料】①已知反应:BaCl2+Na2CO3=2NaCl+BaCO3↓
②部分盐溶液在常温下的pH如下:
【设计方案并进行实验】
请你与他们一起共同完成,并回答所给问题.
| 实验步骤 | 实验现象 | 实验结论 |
| ①称取上述氢氧化钠固体样品8.0g溶于50mL,水配成溶液,向溶液中滴加氯化钡溶液至过量,充分反应后,静置. | 产生白色沉淀 | 说明久置固体中,一定含有 Na2CO3(填化学式). |
| ②用玻璃棒蘸取少量①中充分反应后的上层清液滴在一小块pH试纸上,与标准比色卡对比,测出pH | pH=11 | 说明久置固体中,还一定含有NaOH(填化学式). |
(4)滴加过量BaCl2溶液的目的是检验并除去碳酸钠
(5)【实验结论】通过实验,说明上述猜想Ⅱ是正确的.
8.除去FeCl2晶体中混有少量CuCl2和CaCO3杂质.应选用的方法是( )
| A. | 加水溶解、过滤、蒸发析出晶体 | |
| B. | 加水溶解,加入适量的AgNO3溶液,过滤,蒸发滤液,析出晶体 | |
| C. | 加水溶解,加入适量的铁粉,搅拌,过滤,蒸发滤液,析出晶体 | |
| D. | 加水溶解,加入适量的烧碱溶液、过滤、蒸发滤液,析出晶体 |
 在学习酸的性质时,同学们发现实验室的工业盐酸呈黄色,老师解释说是里面含有氯化铁的缘故.为测定这瓶工业盐酸中氯化铁的含量(假设不含其他杂质),小明做了如下实验:取20g工业盐酸加入到小烧杯中,然后向小烧杯中不断滴加溶质质量分数为10%的氢氧化钠溶液,同时用电子pH计不断读取反应时的pH,得出如图所示的关系.
在学习酸的性质时,同学们发现实验室的工业盐酸呈黄色,老师解释说是里面含有氯化铁的缘故.为测定这瓶工业盐酸中氯化铁的含量(假设不含其他杂质),小明做了如下实验:取20g工业盐酸加入到小烧杯中,然后向小烧杯中不断滴加溶质质量分数为10%的氢氧化钠溶液,同时用电子pH计不断读取反应时的pH,得出如图所示的关系.