题目内容
16.以电解食盐水为基础制取氯气、氢氧化钠等产品的工业称为“氯碱工业”,它是目前化学工业的重要支柱之一.由于粗盐中含有少量MgCl2、CaCl2、Na2SO4等杂质,不符合电解要求,因此必须经过精制.以粗盐为原料的“氯碱工业”流程如下: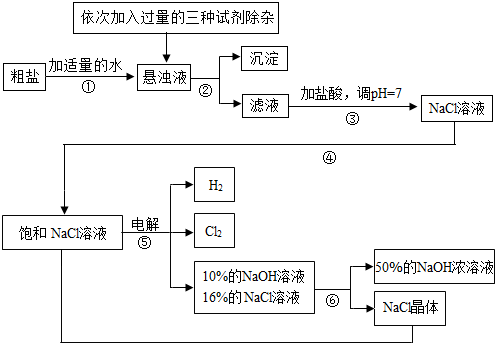
回答下列问题:
(1)操作②的名称是过滤.
(2)操作①②间除杂质时依次加入的三种试剂分别是NaOH溶液、BaCl2溶液Na2CO3溶液、(均过量),写出加入NaOH溶液后发生反应的化学方程式2NaOH+MgCl2=Mg(OH)2↓+2NaCl,其中加入过量Na2CO3溶液的目的是除去剩余的氯化钡和氯化钙.
(3)写出电解饱和NaCl溶液的化学方程式2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑;
(4)该流程中可以循环利用的物质是氯化钠.
分析 (1)根据经过操作②后分出了溶液和固体进行分析;
(2)根据氯化镁和氢氧化钠反应生成氯化钠和氢氧化镁沉淀进行解答;根据氯化钡、碳酸钠所除去的离子和除杂质的原则进行分析;
(3)根据反应物、生成物以及反应条件书写方程式;
(4)根据该反应的流程图进行分析
解答 解:(1)过滤是将固体和液体进行分离的一种操作,故操作②为过滤;
(2)氯化镁和氢氧化钠反应生成氯化钠和氢氧化镁沉淀,化学方程式2NaOH+MgCl2=Mg(OH)2↓+2NaCl;加入氢氧化钠是为了除去氯化镁,加入氯化钡是为了除去硫酸钠,加入碳酸钠是为了除去剩余的氯化钡和氯化钙;
(3)饱和的氯化钠在通电的条件下生成氯化钠、氢气和氯气,故化学方程式为:2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑;
(4)根据装置图可以看出,电解反应后的溶液中依然存在氯化钠,氯化钠蒸发变成饱和状态时又可以电解,所以,该流程中可以循环利用的物质是氯化钠.故答案为:(1)过滤;蒸发; (2)后;氢氧化钡;(3)2NaOH+MgCl2=Mg(OH)2↓+2NaCl;(3)2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑;
(4)氯化钠
点评 本题主要考查了粗盐提纯时的物质的除杂和净化,在除杂质时不要引入新的杂质,了解混合物的分离和除杂的方法.

练习册系列答案
 通城学典默写能手系列答案
通城学典默写能手系列答案
相关题目
6.通过化学变化不可能实现的是( )
| A. | 由分子生成新分子 | B. | 由离子生成新离子 | ||
| C. | 由原子生成新原子 | D. | 由单质生成一种新单质 |
7.在pH=1的溶液中,下列物质能大量共存,且溶液为无色的是( )
| A. | NaOH、NaCl、K2SO4 | B. | MgSO4、Cu(NO)3、KCl | ||
| C. | KNO3、ZnCl2、Ca(NO3)2 | D. | CaCl2、(NH4)2SO4、K2CO3 |
4.化学就在我们身边,它与我们的生活息息相关.
(1)H、O、C、Ca、Na是初中化学常见的几种元素,请选用适当的元素写出符合下列要求的物质的化学式.
①可用作补钙剂的盐是CaCO3; ②可用于温室气体肥料的是CO2;
③可用于改良酸性土壤的碱是Ca(OH)2; ④可用作厨房调味品的有机物是CH3COOH.
(2)、一些食物的近似pH如下表,
请你细心观察分析后回答下列问题:
①苹果汁和葡萄汁相比较,酸性较强的是苹果汁,正常雨水的pH约为5.6的原因水里溶解了二氧化碳.
②人的胃酸中主要成分是盐酸,对于胃酸过多的人,胃液的pH偏小(“偏大”“偏小”或“不变”),空腹时不宜食用上述食物中的酸性食物;在医疗上,治疗胃酸过多的药物之一“胃舒平”其主要成分是氢氧化铝,写出有关化学方程式Al(OH)3+3HCl═AlCl3+3H2O.
(1)H、O、C、Ca、Na是初中化学常见的几种元素,请选用适当的元素写出符合下列要求的物质的化学式.
①可用作补钙剂的盐是CaCO3; ②可用于温室气体肥料的是CO2;
③可用于改良酸性土壤的碱是Ca(OH)2; ④可用作厨房调味品的有机物是CH3COOH.
(2)、一些食物的近似pH如下表,
| 食物 | 苹果 | 葡萄 | 牛奶 | 玉米粥 |
| pH | 2.9~3.3 | 3.5~4.5 | 6.3~6.6 | 6.8~8.0 |
①苹果汁和葡萄汁相比较,酸性较强的是苹果汁,正常雨水的pH约为5.6的原因水里溶解了二氧化碳.
②人的胃酸中主要成分是盐酸,对于胃酸过多的人,胃液的pH偏小(“偏大”“偏小”或“不变”),空腹时不宜食用上述食物中的酸性食物;在医疗上,治疗胃酸过多的药物之一“胃舒平”其主要成分是氢氧化铝,写出有关化学方程式Al(OH)3+3HCl═AlCl3+3H2O.
11.下列叙述正确的是( )
| A. | 将pH试纸浸入溶液中测溶液的pH | |
| B. | 用100 mL的量筒量取5.55 mL的稀硫酸 | |
| C. | 将氢氧化钠固体直接放在托盘天平的托盘上称量 | |
| D. | 粗盐提纯主要步骤是:溶解、过滤、蒸发 |
2.研究小组进行木炭还原氧化铁的探究活动.将木炭、氧化铁及试管充分烘干,并将木炭和氧化铁混合均匀、研磨.取适量上述混合物于试管中,用图1所示的装置加热(试管竖直向上,可使加热时的热量尽少散失).
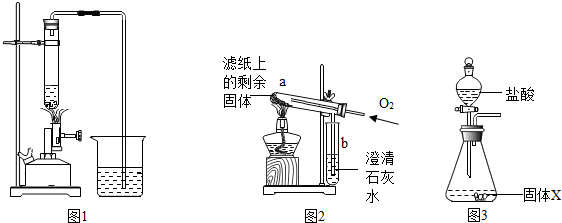
【提出问题】实验结束后,试管中的剩余固体X含有哪些成分,质量分别是多少?
【查阅资料】
铁的氧化物被还原时,是从高价铁的氧化物逐级还原成低价铁的氧化物,最后还原成金属铁.铁的氧化物及其部分性质如下:
Fe2O3为红色固体; Fe3O4和FeO均为黑色固体.其中,Fe3O4具有很好的磁性,能被磁铁吸引.三种氧化物均不溶于水,但能溶于稀盐酸,分别发生如下反应:
Fe2O3+6HCl═2FeCl3+3H₂O
Fe3O4+8HCl═2FeCl3+FeCl2+4H2O
FeO+2HCl═FeCl2+H2O
黄色的FeCl3溶液中滴入无色的KSCN溶液,溶液变为红色,该实验常用于检验FeCl3;FeCl3溶液遇单质铁发生反应:2FeCl3+Fe=3FeCl2,溶液变为浅绿色.
【猜想】固体X可能含有:①Fe ②FeO ③Fe3O4 ④Fe2O3 ⑤C
【实施实验】
目的:确定固体X的组成.
【反思改进】
同学们讨论发现,用上述实验方法不能确定固体X中一定没有Fe3O4,理由是固体X中如果含有Fe3O4,步骤V中加盐酸后,由于铁与FeCl3反应生成FeCl2,遇KSCN溶液也不变血红色.
为确定固体X中是否含Fe3O4并测定其中各成分的质量,同学们又进行了以下实验:
【获得结论】
(1)为确定固体X中是否含Fe3O4,m1~m4中应该用到的数据有m1、m2、m3和m4.
(2)固体X的成分及质量分别是C是1.1g,Fe是16.8g.

【提出问题】实验结束后,试管中的剩余固体X含有哪些成分,质量分别是多少?
【查阅资料】
铁的氧化物被还原时,是从高价铁的氧化物逐级还原成低价铁的氧化物,最后还原成金属铁.铁的氧化物及其部分性质如下:
Fe2O3为红色固体; Fe3O4和FeO均为黑色固体.其中,Fe3O4具有很好的磁性,能被磁铁吸引.三种氧化物均不溶于水,但能溶于稀盐酸,分别发生如下反应:
Fe2O3+6HCl═2FeCl3+3H₂O
Fe3O4+8HCl═2FeCl3+FeCl2+4H2O
FeO+2HCl═FeCl2+H2O
黄色的FeCl3溶液中滴入无色的KSCN溶液,溶液变为红色,该实验常用于检验FeCl3;FeCl3溶液遇单质铁发生反应:2FeCl3+Fe=3FeCl2,溶液变为浅绿色.
【猜想】固体X可能含有:①Fe ②FeO ③Fe3O4 ④Fe2O3 ⑤C
【实施实验】
目的:确定固体X的组成.
| 步骤 | 操作 | 主要现象 | 结论 |
| Ⅰ | 取部分冷却后的固体X倒在滤纸上,用磁铁充分吸引. | 部分固体被吸引到磁铁上 | 可能有Fe或Fe3O4 |
| Ⅱ | 取滤纸上的剩余固体少量,放入图2所示的试管a中,通入氧气,用酒精灯加热. | 固体剧烈燃烧,b中溶液变浑浊 | 一定有C |
| Ⅲ | 另取滤纸上的剩余固体少量,放入试管中,加入足量的稀盐酸. | 无明显现象 | 一定没有FeO和Fe2O3 |
| Ⅳ | 取步骤I磁铁上的固体少量,放入试管中,逐滴加入稀盐酸. | 产生气泡. | 一定有Fe |
| Ⅴ | 在步骤IV所得溶液中逐滴加入KSCN溶液. | 溶液不变红色 | 一定没有Fe3O4 |
同学们讨论发现,用上述实验方法不能确定固体X中一定没有Fe3O4,理由是固体X中如果含有Fe3O4,步骤V中加盐酸后,由于铁与FeCl3反应生成FeCl2,遇KSCN溶液也不变血红色.
为确定固体X中是否含Fe3O4并测定其中各成分的质量,同学们又进行了以下实验:
| 步骤 | 操作 | 数据 |
| Ⅰ | 重新取部分冷却至室温的固体X,称量其质量为m1. | m1=17.9g |
| Ⅱ | 将称量好的固体X全部放入图3所示的锥形瓶中,称量整套装置及药品的质量为m2;打开分液漏斗旋塞,放入足量稀盐酸后关闭旋塞,待没有气泡产生并恢复至室温,再次称量整套装置及药品的质量为m3. | m2=317.9g m3=317.3.g |
| Ⅲ | 将锥形瓶中剩余的固体过滤、洗涤并干燥,称量其质量为m4. | m4=1.1g |
(1)为确定固体X中是否含Fe3O4,m1~m4中应该用到的数据有m1、m2、m3和m4.
(2)固体X的成分及质量分别是C是1.1g,Fe是16.8g.
19.人类的衣、食、住、行都离不开化学科学.下列说法中,合理的是( )
| A. | 化学技术可以提高人类的生活质量 | B. | 化学工业一定会污染环境 | ||
| C. | 自然界中的现象与化学学科无关 | D. | 生活中不需要懂得化学知识 |
20.高铁酸钠(Na2FeO4)是一种新型高效的水处理剂,下列有关高铁酸钠(Na2FeO4)的说法正确的是( )
| A. | 属于氧化物 | |
| B. | 钠、铁、氧三种元素的质量比为2:1:4 | |
| C. | 铁元素的化合价为+6 | |
| D. | 高铁酸钠是由2个钠元素、1个铁元素、4个氧元素组成的物质 |