题目内容
9.享受生活离不开化学知识,家庭厨房就是一个充盈的化学小世界,“柴米油盐酱醋糖”中包含着许多化学内容.(1)下列食物中富含蛋白质的是bc(填序号,可多选).

(2)若锅里的油着火了,要立即盖上锅盖,该灭火原理是隔绝氧气.
(3)厨房中“食用面碱”的主要成分是纯碱,请写出纯碱阴离子的符号C${{O}_{3}}^{2-}$.
(4)随着科技的进步,食品防腐技术也在不断发展.亚硝酸钠(NaNO2)是一种常用的防腐剂,它属于盐(选填“酸、碱、盐、氧化物或有机物”);
(5)打井取用地下水,可用肥皂水区分地下水是软水还是硬水.
(6)农作物生长对土壤酸碱度有一定的要求,常用C测定土壤的酸碱度.
A.紫色石蕊试液 B.无色酚酞试液 C.pH试纸.
分析 (1)根据馒头可以提供糖类,鱼肉、牛肉可以提供蛋白质,蔬菜可以通过维生素进行分析;
(2)根据灭火的原理进行分析;
(3)根据纯碱是碳酸钠,碳酸钠是由钠离子、碳酸根离子构成的进行分析;
(4)根据亚硝酸钠在水中能电离出钠离子和亚硝酸根离子进行分析;
(5)根据肥皂水可以检验软水和硬水进行分析;
(6)根据pH试纸常用来检验溶液的酸碱度进行分析.
解答 解:(1)馒头可以提供糖类,鱼肉、牛肉可以提供蛋白质,蔬菜可以通过维生素,故选:bc;
(2)通过分析灭火的原理可知,锅里的油着火了,要立即盖上锅盖,应用了隔绝氧气;
(3)纯碱是碳酸钠,碳酸钠是由钠离子、碳酸根离子构成的,化学式为:C${{O}_{3}}^{2-}$;
(4)亚硝酸钠在水中能电离出钠离子和亚硝酸根离子,所以亚硝酸钠属于盐;
(5)肥皂水可以检验软水和硬水;
(6)pH试纸常用来检验溶液的酸碱度,故选:C.
故答案为:(1)bc;
(2)隔绝氧气;
(3)C${{O}_{3}}^{2-}$;
(4)盐;
(5)肥皂水;
(6)C.
点评 化学来源于生产、生活,也服务于生产、生活,与生产、生活相关的化学知识,关乎我们的生存、健康和社会的发展,是中考热点之一.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
20.下列括号中对日常生活的变化判断正确的是( )
| A. | 纯净物加热后变为混合物(物理变化) | B. | 玻璃窗破裂(化学变化) | ||
| C. | 用醋酸清洗热水瓶的水垢(物理变化) | D. | 嘴嚼米饭时有甜味(化学变化) |
17.下列对有关物质的性质及其相关用途的叙述正确的是( )
①氧气易溶于水,使得鱼能在水中生存.
②氮气不燃烧也不支持燃烧,难溶于水.
③氧气能支持燃烧,所以可以做火箭的高能燃料.
④氧气能与许多物质发生氧化反应.
①氧气易溶于水,使得鱼能在水中生存.
②氮气不燃烧也不支持燃烧,难溶于水.
③氧气能支持燃烧,所以可以做火箭的高能燃料.
④氧气能与许多物质发生氧化反应.
| A. | ②④ | B. | ①③ | C. | ①②③ | D. | ①②④ |
4.家中烧开水的铝壶和盛放开水的暖瓶,使用时间长了易结水垢.原因是硬水中含有较多的可溶性的钙和镁的化合物,其中碳酸氢钙[Ca(HCO3)2]受热易分解,生成水和大量的气体,还生成一种难溶于水的化合物,它是水垢的主要成分.
[产生问题]碳酸氢钙受热分解除了生成水以外,另外两种生成物是什么?
[提出假设]
①小楠同学认为生成难溶于水的化合物可能是碳酸钙.
②小卓同学认为生成物中的气体可能是二氧化碳.
[实验与事实]依据猜想他们设计了如下实验方案:
[解释与结论]:水垢主要成分之一是碳酸钙.
请写出Ca(HCO3)2受热分解的化学方程式为:Ca(HCO3)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCO3↓+H2O+CO2↑.
[产生问题]碳酸氢钙受热分解除了生成水以外,另外两种生成物是什么?
[提出假设]
①小楠同学认为生成难溶于水的化合物可能是碳酸钙.
②小卓同学认为生成物中的气体可能是二氧化碳.
[实验与事实]依据猜想他们设计了如下实验方案:
| 实验步骤 | 实验现象 | |
| 验证猜想的①方案 | ①把适量难溶于水的化合物置于试管中,滴加稀盐酸 ②把生成的气体通入澄清石灰水中 | 有气泡生成 澄清石灰水变浑浊. |
| 验证猜想②的方案 | 取少量硬水于试管并加热,将生成气体通入 澄清石灰水中 | 澄清石灰水变浑浊 |
请写出Ca(HCO3)2受热分解的化学方程式为:Ca(HCO3)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCO3↓+H2O+CO2↑.
14.为研究锌和铝的金属活动性,某研究小组进行了如下探究.
(1)小明设计的实验方案:向表面积相同的铝片和锌粒中分别加入盐酸.写出铝与盐酸反应的化学方程式:2Al+6HCl═2AlCl3+3H2↑.
(2)小芳将去膜和未去膜的铝片分别放入盐酸中,发现前者比后者反应快,原因是未去膜的铝片表面有Al2O3(填化学式),
(3)小芳在(2)实验中,还观察到有“灰黑色沉淀”这一异常现象出现.
【提出问题】铝与盐酸反应出现的灰黑色沉淀的组成是什么?
【查阅文献】铝在颗粒较小时为灰黑色;氯化铝为无色透明晶体或白色而微带浅黄色的固体,易溶于水和乙醇.
【提出合理假设】假设a:该灰黑色沉淀可能含有铝;
假设b:该灰黑色沉淀可能含有氯化铝和铝;
假设c:该灰黑色沉淀可能含有难溶于酸的物质.
【设计并完成实验】取灰黑色沉淀分别进行如下实验.
【得出结论】由实验①可判断假设c不成立,再集合②和③可得出假设b成立.
(4)若①中小明的实验能比较锌和铝的金属活动性强弱,其所依据的现象是产生气泡的速率,从操作可行性的角度,你认为比较难以控制铝片和锌粒的表面积相同; 从设计方法的角度,你认为还需要控制金属的纯度,盐酸的浓度等变量.
(1)小明设计的实验方案:向表面积相同的铝片和锌粒中分别加入盐酸.写出铝与盐酸反应的化学方程式:2Al+6HCl═2AlCl3+3H2↑.
(2)小芳将去膜和未去膜的铝片分别放入盐酸中,发现前者比后者反应快,原因是未去膜的铝片表面有Al2O3(填化学式),
(3)小芳在(2)实验中,还观察到有“灰黑色沉淀”这一异常现象出现.
【提出问题】铝与盐酸反应出现的灰黑色沉淀的组成是什么?
【查阅文献】铝在颗粒较小时为灰黑色;氯化铝为无色透明晶体或白色而微带浅黄色的固体,易溶于水和乙醇.
【提出合理假设】假设a:该灰黑色沉淀可能含有铝;
假设b:该灰黑色沉淀可能含有氯化铝和铝;
假设c:该灰黑色沉淀可能含有难溶于酸的物质.
【设计并完成实验】取灰黑色沉淀分别进行如下实验.
| 实验编号 | 实验操作 | 实验现象 |
| ① | 加入适量稀盐酸 | 有微量气泡,固体全部溶解,得到澄清溶液 |
| ② | 加入适量蒸馏水 | 固体部分溶解 |
| ③ | 加入适量无水乙醇 | 固体部分溶解 |
(4)若①中小明的实验能比较锌和铝的金属活动性强弱,其所依据的现象是产生气泡的速率,从操作可行性的角度,你认为比较难以控制铝片和锌粒的表面积相同; 从设计方法的角度,你认为还需要控制金属的纯度,盐酸的浓度等变量.
1.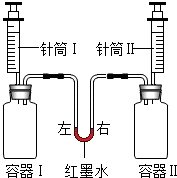 如图所示进行实验,同时将针筒内全部液体迅速注入容器中.实验内容如下表所示.
如图所示进行实验,同时将针筒内全部液体迅速注入容器中.实验内容如下表所示.
实验开始前红墨水左右两端液面保持相平,容器Ⅰ、Ⅱ体积相同,装置气密性良好.
(1)实验a中,容器Ⅰ内产生的现象是澄清石灰水变浑浊.
红墨水液面位置发生变化的原因是Ca(OH)2+CO2═CaCO3↓+H2O (用化学方程式表示).
(2)实验b中,针筒Ⅰ、Ⅱ内盐酸足量且溶质质量分数相同,产生气泡更剧烈的是容器Ⅱ (填“Ⅰ”或“Ⅱ”).红墨水液面位置变化情况是先是左高右低,最终红墨水左右两端液面保持相平.反应结束并恢复到原来的温度后,两边的红墨水保持相平.
 如图所示进行实验,同时将针筒内全部液体迅速注入容器中.实验内容如下表所示.
如图所示进行实验,同时将针筒内全部液体迅速注入容器中.实验内容如下表所示.实验开始前红墨水左右两端液面保持相平,容器Ⅰ、Ⅱ体积相同,装置气密性良好.
| 实验 编号 | 容器I | 针筒I | 容器Ⅱ | 针筒Ⅱ | 红墨水 液面位置 |
| a | 10mL 水 | NaCl | 10mL 水 | 保持 左高右低 | |
| b | 二氧化碳 (充满) | 10mL 澄清石灰水 | 二氧化碳 (充满) | 10mlL浓氢氧化钠溶液 | |
| c | 1g锌 | 15mL盐酸 | 1g镁 | 15mL盐酸 |
红墨水液面位置发生变化的原因是Ca(OH)2+CO2═CaCO3↓+H2O (用化学方程式表示).
(2)实验b中,针筒Ⅰ、Ⅱ内盐酸足量且溶质质量分数相同,产生气泡更剧烈的是容器Ⅱ (填“Ⅰ”或“Ⅱ”).红墨水液面位置变化情况是先是左高右低,最终红墨水左右两端液面保持相平.反应结束并恢复到原来的温度后,两边的红墨水保持相平.
 为测定空气中氧气的体积含量如图所示,根据要求回答问题:
为测定空气中氧气的体积含量如图所示,根据要求回答问题: 二氧化碳若合理利用,是一种重要的原料.
二氧化碳若合理利用,是一种重要的原料.