题目内容
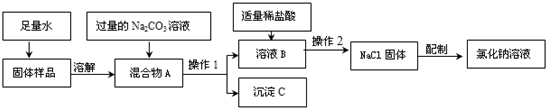
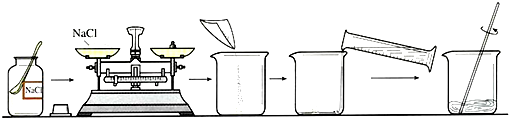
22、要配制50g质量分数为20%的食盐溶液.现提供25g质量分数为40%的食盐溶液、20g质量分数为15%的食盐溶液及足够多的固体食盐和水,请选用上述药品,设计不同的配制方案填入下表:
方案一:10gNaCl,40mL水
方案二:25g40%NaCl,25mL水
方案三:20g15%NaCl,7gNaCl,23g水
方案二:25g40%NaCl,25mL水
方案三:20g15%NaCl,7gNaCl,23g水

分析:根据所需配制的溶液计算出配制时所需要溶质和溶剂的质量,然后利用所提供的药品设计不同的配制所需溶液的方法.
解答:解:配制50g质量分数为20%的食盐溶液需要食盐的质量=50g×20%=10g,则需要水的质量=50g-10g=40g(合40mL);
可以直接称10g食盐、量取40mL水,混合溶解所得溶液即为所需配制的溶液;
可取40%的溶液加水稀释进行配制,需要40%的溶液的质量=10g÷40%=25g,加水的量=50g-25g(合25mL);
20g质量分数为15%的食盐溶液中食盐质量=20g×15%=3g,因此,可取20g15%的溶液再加10g-3g=7g食盐和50g-20g-7g=23g(合23mL)水进行配制;
故答案为:方案一:10gNaCl,40mL水;方案二:25g40%NaCl,25mL水;方案三:20g15%NaCl,7gNaCl,23g水.
可以直接称10g食盐、量取40mL水,混合溶解所得溶液即为所需配制的溶液;
可取40%的溶液加水稀释进行配制,需要40%的溶液的质量=10g÷40%=25g,加水的量=50g-25g(合25mL);
20g质量分数为15%的食盐溶液中食盐质量=20g×15%=3g,因此,可取20g15%的溶液再加10g-3g=7g食盐和50g-20g-7g=23g(合23mL)水进行配制;
故答案为:方案一:10gNaCl,40mL水;方案二:25g40%NaCl,25mL水;方案三:20g15%NaCl,7gNaCl,23g水.
点评:解决本题抓住关键点:配制需要10g食盐和40g水,只要设法满足这一要求,所设计的方案就是可行的.

练习册系列答案
相关题目
要配制50g质量分数为20%的食盐溶液.现提供25g质量分数为40%的食盐溶液、20g质量分数为15%的食盐溶液及足够多的固体食盐和水,请选用上述药品,设计不同的配制方案填入下表:
| 配制方案(只要说明配制时所需的各种药品用量) | |
| 方案一 | ________ |
| 方案二 | ________ |
| 方案三 | ________ |
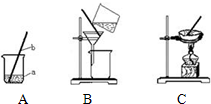 (1)在做粗盐初步提纯的实验时,要进行如图所示的实验操作.
(1)在做粗盐初步提纯的实验时,要进行如图所示的实验操作.