题目内容
12.盐类是重要的化工原料.(1)碳酸钠能与下列物质反应:①稀盐酸②氢氧化钙③氯化钙
①上述三个反应中,体现了相同反应本质的两个反应是②③(填编号).
②利用碳酸钠除去氯化钠中少量氯化钙的实验中,不能(填“能”或“不能”)用碳酸钾代替碳酸钠.
(2)检验铵盐的方法是:取样,加入少量熟石灰,混合,研磨,有刺激性气味的气体生成时,说明该固体为铵盐.请写出硝酸铵与熟石灰反应的方程式:2NH4NO3+Ca(OH)2═Ca(NO3)2+2H2O+2NH3↑.
分析 (1)①根据碳酸钠能与稀盐酸反应生成氯化钠、水和二氧化碳,能与氢氧化钙、氯化钙反应生成碳酸钙白色沉淀,据此进行分析解答.
②除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
(2)根据铵盐与碱性物质混合后能放出有刺激性气味的气体,进行分析解答.
硝酸铵与熟石灰反应生成硝酸钙、水和氨气,写出反应的化学方程式即可.
解答 解:(1)①碳酸钠能与稀盐酸反应生成氯化钠、水和二氧化碳,能与氢氧化钙、氯化钙反应生成碳酸钙白色沉淀,上述三个反应中,体现了相同反应本质的两个反应是②③,反应实质是碳酸根离子和钙离子生成碳酸钙白色沉淀.
②利用碳酸钠除去氯化钠中少量氯化钙的实验中,不能利用碳酸钾代替碳酸钠,因为碳酸钾能与氯化钙反应生成碳酸钙沉淀和氯化钾,能除去杂质但引入了新的杂质氯化钾,不符合除杂原则.
(2)检验铵盐的方法是:取样,加入少量熟石灰,混合,研磨,有刺激性气味的气体产生,说明该固体为铵盐.
硝酸铵与熟石灰反应生成硝酸钙、水和氨气,反应的化学方程式为:2NH4NO3+Ca(OH)2═Ca(NO3)2+2H2O+2NH3↑.
故答案为:(1)①、②③;②不能;
(2)刺激性气味的气体生成;2NH4NO3+Ca(OH)2═Ca(NO3)2+2H2O+2NH3↑.
点评 本题难度不大,掌握盐的化学性质、检验铵盐的方法、抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.

练习册系列答案
相关题目
2.生活中的下列做法节能、健康、环保的是( )
| A. | 常吃烧烤食品 | B. | 常用太阳能热水洗澡 | ||
| C. | 常坐私家车出行 | D. | 常把食品包装袋丢弃 |
3.今年“两会”上,环保部长说:每天起来第一件事情就是看天.原因就是雾霾惹的祸.下列不利于治理雾霾的是( )
| A. | 13年9月,国务院出台《大气污染防治行动计划》 | |
| B. | 14年,李克强总理在政府工作报告中提出,要像向贫困宣战一样向污染宣战 | |
| C. | 大力增加除尘改造,如煤改气工程 | |
| D. | 恶劣的自然天气加上人为破坏引起的沙尘暴 |
7.下列事实和解释相符的是( )
| A. | 干冰用作制冷剂-干冰是冰 | |
| B. | 用炭黑墨汁书写的字经久不变色-常温下,碳的化学性质稳定 | |
| C. | 纯碱溶液使酚酞变红-纯碱是碱 | |
| D. | 制糖工业用活性炭脱色制白糖-活性炭和有色物质反应 |
17.下列各组物质中,都由离子构成的一组是( )
| A. | 金和金刚石 | B. | 水和氨气 | C. | 碳酸钠和氯化钠 | D. | 干冰和硫酸铜 |
1.下列关于气体的收集方法说法正确的是( )
| A. | 因为CO2能溶于水,所以不能用排水法收集 | |
| B. | 用排水法可以直接收集到纯净且干燥的氢气 | |
| C. | 因为常温时NO和O2反应生成NO2,所以不能用排空气法收集NO | |
| D. | 因为CO有毒,所以不能用排空气法收集 |

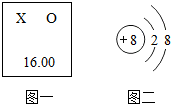 如图所示某元素在周期表中和其粒子结构的相关信息,试回答相关问题
如图所示某元素在周期表中和其粒子结构的相关信息,试回答相关问题