题目内容
把Cu、Fe、Zn同时放入一定量的硫酸铜溶液中充分反应后,溶液为浅绿色,过滤,滤纸上 一定有 ,可能有 .滤液中一定有 ,肯定没有 .
考点:金属的化学性质
专题:金属与金属材料
分析:锌比铁活泼,铁比铜活泼,把Cu、Fe、Zn同时放入一定量的硫酸铜溶液中时,锌先和硫酸铜反应生成硫酸锌和铜,当锌完全反应后,如果硫酸铜有剩余,则铁和硫酸铜反应生成硫酸亚铁和铜;
硫酸锌溶液是无色溶液,硫酸亚铁溶液是浅绿色溶液,硫酸铜是蓝色溶液.
硫酸锌溶液是无色溶液,硫酸亚铁溶液是浅绿色溶液,硫酸铜是蓝色溶液.
解答:解:把Cu、Fe、Zn同时放入一定量的硫酸铜溶液中充分反应后,溶液为浅绿色,说明锌完全反应,硫酸铜也完全反应,铁和硫酸铜反应生成了浅绿色的硫酸亚铁溶液,但是铁是否完全反应则无法确定,因此过滤,滤纸上一定有Cu,可能有Fe,滤液中一定有ZnSO4、FeSO4,肯定没有CuSO4.
故填:Cu;Fe;ZnSO4、FeSO4;CuSO4.
故填:Cu;Fe;ZnSO4、FeSO4;CuSO4.
点评:要会利用金属活动顺序表分析实验,氢前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出来.

练习册系列答案
相关题目
用分子的观点解释下列现象,错误的是( )
| A、热胀冷缩-----------分子大小随温度的变化而改变 |
| B、花香四溢-----------分子不断地运动 |
| C、食物腐败------------分子发生变化 |
| D、酒精挥发-------------分子间间隔变大 |
氧气由( )
| A、氧元素组成 |
| B、氧原子构成 |
| C、两个氧元素组成 |
| D、两个氧原子构成 |
下列粒子中,能保持水的化学性质的是( )
| A、水分子 | B、氢原子 |
| C、氧原子 | D、氢原子和氧原子 |
在硫酸锌和硫酸铜混合液中加入过量铁粉充分反应后,过滤,留在滤纸上的是( )
| A、Cu |
| B、Zn |
| C、Zn Cu |
| D、Fe Cu |


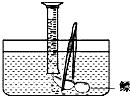 小明对妈妈杀鱼时从鱼肚内取出的鳔产生了兴趣,他确定了“探究鳔内气体体积和成分”作为研究性学习的课题.小明通过查阅有关资料获知:这种鱼鳔内氧气约占
小明对妈妈杀鱼时从鱼肚内取出的鳔产生了兴趣,他确定了“探究鳔内气体体积和成分”作为研究性学习的课题.小明通过查阅有关资料获知:这种鱼鳔内氧气约占