题目内容
将113gNa2CO3溶液与131gCaCl2溶液混合后恰好完全反应.过滤得到滤液的质量为234g.试求:
(1)反应生成沉淀的质量.
(2)所得滤液中溶质的质量分数.
解:根据题意知生成Ca CO3沉淀的质量为:113g+131g-234g=10g
设:反应生成NaCl的质量为x
Na2CO3 +CaCl2=2NaCl+CaCO3↓
2×58.5 100
x 10g
 ,
,
x=11.7g
所得滤液中溶质的质量分数为: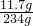 ×100%=5%
×100%=5%
答:生成沉淀的质量为l0g,所得滤液中溶质的质量分数为5%
分析:(1)分析题意可知,滤液减少的质量就是生成沉淀的质量;
(2)利用碳酸钠与氯化钙反应的化学方程式和生成沉淀的质量,列出比例式,就可计算出反应生成氯化钠的质量,然后根据“溶质质量分数=溶质质量÷溶液质量×100%”计算即可.
点评:本题主要考查学生运用化学方程式和溶质质量分数公式综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.
设:反应生成NaCl的质量为x
Na2CO3 +CaCl2=2NaCl+CaCO3↓
2×58.5 100
x 10g
 ,
,x=11.7g
所得滤液中溶质的质量分数为:
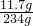 ×100%=5%
×100%=5% 答:生成沉淀的质量为l0g,所得滤液中溶质的质量分数为5%
分析:(1)分析题意可知,滤液减少的质量就是生成沉淀的质量;
(2)利用碳酸钠与氯化钙反应的化学方程式和生成沉淀的质量,列出比例式,就可计算出反应生成氯化钠的质量,然后根据“溶质质量分数=溶质质量÷溶液质量×100%”计算即可.
点评:本题主要考查学生运用化学方程式和溶质质量分数公式综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.

练习册系列答案
相关题目
一个密闭容器中加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,测得数据见下表.下列说法中正确的是
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前质量 | 8g | 35g | 5g | 8g |
| 反应后质量 | 2g | X | 5g | 42g |
- A.丁可能是化合物
- B.在该反应中,丙物质一定做催化剂
- C.该反应是化合反应
- D.在该反应的化学方程式中,甲、乙的化学计量数之比为3:l4
 Fe2O3+________SO2
Fe2O3+________SO2