题目内容
某物质在空气中完全燃烧生成二氧化碳和水的质量比为44:27,则关于这种物质的组成描述正确的是
- A.该物质只含碳元素,氢元素
- B.该物质中碳元素与氢元素的质量比为12:1
- C.该物质中一定含有碳元素和氢元素,可能含有氧元素
- D.该物质的分子中碳原子与氢原子的个数比为1:2
C
分析:在化学反应中,反应前后原子的种类没有改变,数目没有增减,原子的质量也没有改变,所以反应前后物质的质量总和相等.根据生成物CO2和H2O中C、H元素质量,可以确定可燃物中C、H元素比和原子个数比.
解答:A、生成物中含有C、H、O三种元素,所以可燃物中一定含C、H元素,但是否含有O元素在此无法判断,故A说法不正确;
B、由于生成的二氧化碳和水的质量比为:44:27,所以可以设二氧化碳的质量为44g而水的质量为27g,则:
44gCO2中C元素质量=44g×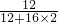 ×100%=12g;
×100%=12g;
27gH2O中H元素质量=27g× ×100%=3g,所以可燃物中C、H元素质量比=12g:3g=4:1,故B说法不正确;
×100%=3g,所以可燃物中C、H元素质量比=12g:3g=4:1,故B说法不正确;
C、生成物中含有C、H、O三种元素,所以可燃物中一定含C、H元素,可燃物中是否含O元素无法判断,所以只能说可能含O元素.故C说法正确;
D、利用原子个数比可求得可燃物中C、H原子个数比= :
: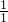 =1:3,故D说法不正确.
=1:3,故D说法不正确.
故选C.
点评:本题主要考查有关化学式的计算,难度稍大.关键是找到确定该物质的元素组成、元素质量和原子个数比的方法.
分析:在化学反应中,反应前后原子的种类没有改变,数目没有增减,原子的质量也没有改变,所以反应前后物质的质量总和相等.根据生成物CO2和H2O中C、H元素质量,可以确定可燃物中C、H元素比和原子个数比.
解答:A、生成物中含有C、H、O三种元素,所以可燃物中一定含C、H元素,但是否含有O元素在此无法判断,故A说法不正确;
B、由于生成的二氧化碳和水的质量比为:44:27,所以可以设二氧化碳的质量为44g而水的质量为27g,则:
44gCO2中C元素质量=44g×
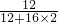 ×100%=12g;
×100%=12g; 27gH2O中H元素质量=27g×
 ×100%=3g,所以可燃物中C、H元素质量比=12g:3g=4:1,故B说法不正确;
×100%=3g,所以可燃物中C、H元素质量比=12g:3g=4:1,故B说法不正确;C、生成物中含有C、H、O三种元素,所以可燃物中一定含C、H元素,可燃物中是否含O元素无法判断,所以只能说可能含O元素.故C说法正确;
D、利用原子个数比可求得可燃物中C、H原子个数比=
 :
: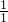 =1:3,故D说法不正确.
=1:3,故D说法不正确.故选C.
点评:本题主要考查有关化学式的计算,难度稍大.关键是找到确定该物质的元素组成、元素质量和原子个数比的方法.

练习册系列答案
相关题目
(6分)元素组成物质。根据给定元素回答下列问题。
已知:下列物质由氢、碳、氧、磷、钙、钠、铁中的一种或几种元素组成
(1)若某固体在完全燃烧和不完全燃烧时,分别生成甲、乙不同的气体。则该固体的化学式为________。为鉴别甲乙气体,下述方法可行的是___________。(填字母序号)
| a.分别用燃着木条检验 | b.分别通入澄清石灰水中 |
| c.分别通入水中 | d.分别通入石蕊试液中 |
(3)若A、B两种物质组成元素相同A→B→C,则B生成C的化学方程式为_______________________________。
(4)若某物质与盐酸反应生成使澄清石灰水变浑浊的气体,则该物质中一定含____元素。
(5)若某元素单质与稀盐酸反应生成化合物A,又知B与A组成元素相同。工业上用B
和H2在300-350℃时反应可制得A和盐酸,该反应的化学方程式为_______________________________。
元素组成物质.根据给定元素回答下列问题.
已知:下列物质由氢、碳、氧、磷、钙、钠、铁中的一种或几种元素组成
(1)若某固体在完全燃烧和不完全燃烧时,分别生成甲、乙不同的气体.则该固体的化学式为 .为鉴别甲乙气体,下述方法可行的是 .(填字母序号)
(2)若某物质在空气中燃烧产生大量白烟.则此反应的化学方程式为 .
(3)若A、B两种物质组成元素相同A→B→C,则B生成C的化学方程式为 .
(4)若某物质与盐酸反应生成使澄清石灰水变浑浊的气体,则该物质中一定含 元素.
(5)若某元素单质与稀盐酸反应生成化合物A,又知B与A组成元素相同.工业上用B和H2,在300-350℃时反应可制得A和盐酸,该反应的化学方程式为 .
已知:下列物质由氢、碳、氧、磷、钙、钠、铁中的一种或几种元素组成
(1)若某固体在完全燃烧和不完全燃烧时,分别生成甲、乙不同的气体.则该固体的化学式为 .为鉴别甲乙气体,下述方法可行的是 .(填字母序号)
| a.分别用燃着木条检验 | b.分别通入澄清石灰水中 |
| c.分别通入水中 | d.分别通入石蕊试液中 |
(3)若A、B两种物质组成元素相同A→B→C,则B生成C的化学方程式为 .
(4)若某物质与盐酸反应生成使澄清石灰水变浑浊的气体,则该物质中一定含 元素.
(5)若某元素单质与稀盐酸反应生成化合物A,又知B与A组成元素相同.工业上用B和H2,在300-350℃时反应可制得A和盐酸,该反应的化学方程式为 .