题目内容
纯度为70%的赤铁矿60吨,在冶炼过程中损失铁2%,问能炼出含杂质4%的生铁多少吨?
考点:含杂质物质的化学反应的有关计算
专题:有关化学方程式的计算
分析:由赤铁矿的质量和氧化铁的质量分数以及生铁中杂质的质量分数,根据赤铁矿炼铁的化学方程式可以计算出炼出生铁的质量.
解答:解:设可炼出铁的质量为x,
Fe2O3+3CO
2Fe+3CO2
160 112
60t×70% x
x=29.4t
能炼出含杂质4%的生铁=
=30.125t
答案:能炼出含杂质4%的生铁30.125t
Fe2O3+3CO
| ||
160 112
60t×70% x
x=29.4t
能炼出含杂质4%的生铁=
| 29.4t(1-2%) |
| 96% |
答案:能炼出含杂质4%的生铁30.125t
点评:本题主要考查含杂质物质的化学方程式的计算,难度稍大.

练习册系列答案
 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案
相关题目
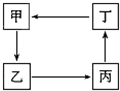 甲、乙、丙、丁四种物质有如图所示的转化关系(“→”表示物质间存在转化关系,部分反应物和产物已略去),则甲、乙、丙、丁依次是( )
甲、乙、丙、丁四种物质有如图所示的转化关系(“→”表示物质间存在转化关系,部分反应物和产物已略去),则甲、乙、丙、丁依次是( )| A、CO2、Ca(OH)2、CaCO3、HCl |
| B、H2O、O2、CO2、H2CO3 |
| C、CO、CO2、CaCO3、HCl |
| D、C、CO、CO2、H2CO3 |