题目内容
某物质x可发生如下变化:x
y
x,则x可能是( )
| +H2SO4 |
| NaOH |
| A.CuO | B.Na2C03 | C.Fe203 | D.Cu(OH)2 |
分别将四个选项从左X处代入;
A、CuO与稀硫酸反应生成CuSO4,硫酸铜与NaOH反应生成氢氧化铜沉淀和硫酸钠,故A不正确;
B、Na2C03与稀硫酸反应生成Na2SO4、H20、CO2,二氧化碳能与氢氧化钠溶液反应生成碳酸钠,故B正确;
C、Fe203与稀硫酸反应生成硫酸铁,硫酸铁与NaOH反应生成氢氧化铁沉淀和硫酸钠,故C不正确;
D、Cu(OH)2与稀硫酸反应生成CuSO4,CuSO4与NaOH反应生成氢氧化铜沉淀和硫酸钠,故D正确;
故选BD
A、CuO与稀硫酸反应生成CuSO4,硫酸铜与NaOH反应生成氢氧化铜沉淀和硫酸钠,故A不正确;
B、Na2C03与稀硫酸反应生成Na2SO4、H20、CO2,二氧化碳能与氢氧化钠溶液反应生成碳酸钠,故B正确;
C、Fe203与稀硫酸反应生成硫酸铁,硫酸铁与NaOH反应生成氢氧化铁沉淀和硫酸钠,故C不正确;
D、Cu(OH)2与稀硫酸反应生成CuSO4,CuSO4与NaOH反应生成氢氧化铜沉淀和硫酸钠,故D正确;
故选BD

练习册系列答案
 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案
相关题目
兴化地处里下河地区,河港纵横,水系发达.但河水中含有较多的碳酸氢钙[Ca(HCO3)2],水的硬度较大.(查阅资料:碳酸氢钙易溶于水.当溶有碳酸氢钙的水遇热时,溶解在水里的碳酸氢钙就会发生分解,生成碳酸钙沉积下来,这就形成了水垢Ca(HCO3)2△CaCO3↓+H2O+CO2↑).已知碳酸氢钠、碳酸氢钾、碳酸氢镁等物质均能在加热条件下发生类似的反应.而碳酸钠、碳酸钾则在通常情况下比较稳定,加热不分解.
请你根据上述信息完成下列各题:
(1)根据上述信息可知,水垢的主要成分是 .你能用什么方法来除去水垢?(用化学方程式表示) .
(2)若碳酸镁粉末中混有少量的碳酸氢镁,请写出除去杂质碳酸氢镁的方法(用化学方程式表示) .
(3)实验室有两包质量均为10.6g的固体,分别是碳酸钠和碳酸氢钠.现分别经如下处理:①充分加热 ②滴加足量的稀盐酸 ③将两步反应生成的气体全部收集后通入足量的澄清石灰水.则生成沉淀的质量 (填“相等”、“不相等”或“无法判断”).
(4)在加热条件下密闭容器内发生某一化学反应,现对反应体系内的X、Y、Z、Q四种物质进行测定,测得数据如下:
请回答下列问题:
①上表中的”待测数据”的数值是 .
②此密闭容器内反应类型属于 (填基本反应类型).
③若X是水,Q是能使澄清石灰水变浑浊的气体,且X、Y、Z、Q四种物质的化学计量数之比为1:1:2:1,则物质Y的相对分子质量为 .
(5)实验室制取二氧化碳时若不慎使用了浓盐酸,生成的气体中除混有水蒸气外还可能混有 气体,这是因为浓盐酸具有 性.
现要除去杂质气体,可采用如图所示的装置把不纯的气体进行洗气.
①不纯气体应从 (填“a”或“b”)端通入.
②若只需要把生成的气体干燥,可在瓶中盛放 .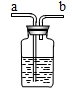
③可在瓶中盛放饱和的碳酸氢钠溶液除去另一种杂质气体.写出有关反应的化学方程式 .
请你根据上述信息完成下列各题:
(1)根据上述信息可知,水垢的主要成分是
(2)若碳酸镁粉末中混有少量的碳酸氢镁,请写出除去杂质碳酸氢镁的方法(用化学方程式表示)
(3)实验室有两包质量均为10.6g的固体,分别是碳酸钠和碳酸氢钠.现分别经如下处理:①充分加热 ②滴加足量的稀盐酸 ③将两步反应生成的气体全部收集后通入足量的澄清石灰水.则生成沉淀的质量
(4)在加热条件下密闭容器内发生某一化学反应,现对反应体系内的X、Y、Z、Q四种物质进行测定,测得数据如下:
| 物质 | X | Y | Z | Q |
| 反应前质量(g) | 40.0 | 4.6 | 37.8 | 0.0 |
| 反应后质量(g) | 43.6 | 待测数据 | 4.2 | 8.8 |
①上表中的”待测数据”的数值是
②此密闭容器内反应类型属于
③若X是水,Q是能使澄清石灰水变浑浊的气体,且X、Y、Z、Q四种物质的化学计量数之比为1:1:2:1,则物质Y的相对分子质量为
(5)实验室制取二氧化碳时若不慎使用了浓盐酸,生成的气体中除混有水蒸气外还可能混有
现要除去杂质气体,可采用如图所示的装置把不纯的气体进行洗气.
①不纯气体应从
②若只需要把生成的气体干燥,可在瓶中盛放

③可在瓶中盛放饱和的碳酸氢钠溶液除去另一种杂质气体.写出有关反应的化学方程式
请你用所学知识解释以下生活中的问题:
(1)糖类、油脂、蛋白质和维生素都是人类的基本营养物质.下表为某品牌燕麦片标签中的一部分.
| 每100g含有 营养成分 | 糖类 | 油脂 | 蛋白质 | 维生素C | 钙 | 镁 | 钠 | 锌 |
| 7.6g | 7.8g | 7.4g | 18mg | 201mg | 18.2mg | 30.8mg | 8.1mg |
②维生素C易溶于水,向其水溶液中滴入紫色石蕊试液,石蕊变红色,加热该溶液至沸腾,红色消失.因此,烹调富含维生素C的食物时,应该注意______;在碱性条件下,维生素C易被空气氧化,烧煮时最好加一点______.
(2)为抵抗去冬今春华北地区大旱,党中央组织各级政府积极打井汲取地下水帮助百姓度过难关.饮用遭到污染或硬度大的地下水不利于人体健康.为此我们还应对其进行进一步的处理.
①测定地下水的酸碱度,方法是______.
②地下水经过沉淀后,还必须对其进行消毒.我们通常使用漂白粉,其有效成分次氯酸钙可发生如下反应:Ca(ClO)2+X+H2O=CaCO3↓+2HClO,则X的化学式为______.
请你用所学知识解释以下生活中的问题:
(1)糖类、油脂、蛋白质和维生素都是人类的基本营养物质。下表为某品牌燕麦片标签中的一部分。
| 每100 g含有 营养成分 | 糖类 | 油脂 | 蛋白质 | 维生素C | 钙 | 镁 | 钠 | 锌 |
| 7.6 g | 7.8 g | 7.4 g | 18 mg | 201 mg | 18.2 mg | 30.8 mg | 8.1 mg |
① 燕麦片的营养成分中能与水反应生成氨基酸的营养物质是________________;每克营养物质氧化时放出能量最多的是_________ ;人体必需的微量元素是_______________。
;人体必需的微量元素是_______________。
② 维生素C易溶于水,向其水溶液中滴入紫色石蕊试液,石蕊变红色,加热该溶液至沸腾,红色消失。因此,烹调富含维生素C的食物时,应该注意_____________;在碱性条件下,维生素C易被空气氧化,烧煮时最好加一点________。
(2)为抵抗去冬今春华北地区大旱,党中央组织各级政府积极打井汲取地下水帮助百姓度过难关。饮用遭到污染或硬度大的地下水不利于人 体健康。为此我们还应对其进行进一步的处理。
体健康。为此我们还应对其进行进一步的处理。
①测定地下水的酸碱度,方法是___________________________________ _________。
_________。
②地下水经过沉淀后,还 必须对其进行消毒。我们通常使用漂白粉,其有效成分次氯酸钙可发生如下反应: Ca(ClO)2+X+H2O=CaCO3↓+2HClO,则X的化学式为 。
必须对其进行消毒。我们通常使用漂白粉,其有效成分次氯酸钙可发生如下反应: Ca(ClO)2+X+H2O=CaCO3↓+2HClO,则X的化学式为 。