题目内容
(1)从图可知,加入的NaOH先跟滤液中______反应,后跟______反应.(写化学式)(2)该样品中CuO的质量是______.
(3)计算所加氢氧化钠溶液中溶质的质量分数.(写出计算过程)
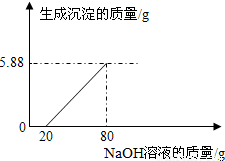
【答案】分析:(1)由图象可知氢氧化钠放入后开始并没有沉淀产生,所以反应开始时是氢氧化钠先与盐酸的反应;
(2)依据质量守恒定律可知该过程的反应中铜元素的质量不会变化,所以可以建立氧化铜与氯化铜的关系式求出氧化铜的质量;
(3)依据氢氧化钠和氯化铜的反应方程式根据沉淀的质量可求反应的氢氧化钠质量,进而求出氢氧化钠的溶质质量分数;
解答:解:(1)氢氧化钠放入后开始并没有沉淀产生,所以加入的NaOH先跟滤液中的盐酸反应再和溶液中的氯化铜反应生成氢氧化铜的沉淀;
(2)依据方程式CuO+2HCl═CuCl2+H2O和CuCl2+2NaOH═Cu(OH)2↓+2NaCl可知每个氧化铜的分子最终可以生成1个氢氧化铜分子,所以可建立关系式CuO~Cu(OH)2;
设样品中氧化铜的质量是x
CuO~Cu(OH)2
80 98
x 5.88g
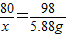
x=4.8g
(3)设与氯化铜反应的氢氧化钠的质量是y
CuCl2+2NaOH═Cu(OH)2↓+2NaCl
80 98
y 5.88g
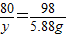
y=4.8g
所以氢氧化钠溶液中溶质的质量分数=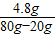 ×100%=8%
×100%=8%
故答案为:(1)HCl;CuCl2;(2)4.8g;(3)答:氢氧化钠溶液中溶质的质量分数为8%;
点评:此题是对化学方程式计算的考查,解题的关键是能够对题中所发生反应的过程有较清晰的把握,依据化学反应中元素的质量不变进行解题往往能简化计算的过程,从而起到事半功倍的效果.
(2)依据质量守恒定律可知该过程的反应中铜元素的质量不会变化,所以可以建立氧化铜与氯化铜的关系式求出氧化铜的质量;
(3)依据氢氧化钠和氯化铜的反应方程式根据沉淀的质量可求反应的氢氧化钠质量,进而求出氢氧化钠的溶质质量分数;
解答:解:(1)氢氧化钠放入后开始并没有沉淀产生,所以加入的NaOH先跟滤液中的盐酸反应再和溶液中的氯化铜反应生成氢氧化铜的沉淀;
(2)依据方程式CuO+2HCl═CuCl2+H2O和CuCl2+2NaOH═Cu(OH)2↓+2NaCl可知每个氧化铜的分子最终可以生成1个氢氧化铜分子,所以可建立关系式CuO~Cu(OH)2;
设样品中氧化铜的质量是x
CuO~Cu(OH)2
80 98
x 5.88g
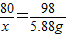
x=4.8g
(3)设与氯化铜反应的氢氧化钠的质量是y
CuCl2+2NaOH═Cu(OH)2↓+2NaCl
80 98
y 5.88g
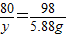
y=4.8g
所以氢氧化钠溶液中溶质的质量分数=
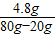 ×100%=8%
×100%=8%故答案为:(1)HCl;CuCl2;(2)4.8g;(3)答:氢氧化钠溶液中溶质的质量分数为8%;
点评:此题是对化学方程式计算的考查,解题的关键是能够对题中所发生反应的过程有较清晰的把握,依据化学反应中元素的质量不变进行解题往往能简化计算的过程,从而起到事半功倍的效果.

练习册系列答案
 课课优能力培优100分系列答案
课课优能力培优100分系列答案 优百分课时互动系列答案
优百分课时互动系列答案
相关题目
 (2012?茂名)(1)从图可知,加入的NaOH先跟滤液中
(2012?茂名)(1)从图可知,加入的NaOH先跟滤液中

 (1)从图可知,加入的NaOH先跟滤液中______反应,后跟______反应.(写化学式)
(1)从图可知,加入的NaOH先跟滤液中______反应,后跟______反应.(写化学式)