题目内容
维生素C(C6H1206)主要存在于蔬菜水果中,他能促进人体生长发育.
(1)维生素C的相对分子质量为
(2)计算88g维生素C中含碳元素的质量为 g.
【考点】相对分子质量的概念及其计算;化合物中某元素的质量计算.
【专题】化学式的计算;有关化学式的计算.
【分析】(1)根据相对分子质量为构成分子的各原子的相对原子质量之和,进行分析解答.
(2)根据化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答.
【解答】解:(1)维生素C的相对分子质量为6×12+8×1+6×16=176.
(2)176g维生素C中碳元素的质量为88g×
 ×100%=36g.
×100%=36g.
故答案为:(1)176;(2)36g.
【点评】本题难度不大,考查同学们灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.
27.在做“氢气还原氧化铜”的实验中,将8g氧化铜放入试管中,通入足量的氢气并加热一段时间.再次称量固体时,发现剩余固体的质量为7.2g,问生成铜的质量为多少?
【考点】根据化学反应方程式的计算.
【专题】有关化学方程式的计算.
【分析】根据氢气和氧化铜在加热的条件下生成铜和水,固体减少的质量是氧元素的质量,然后结合化学方程式进行解答.
【解答】解:通过分析题意可知,固体减少质量为:8﹣7.2=0.8g,
设生成铜的质量为x,
CuO+H2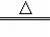
 Cu+H2O 固体减少
Cu+H2O 固体减少
80 64 16
x 0.8g
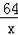
 =
=

x=3.2g
答:生成铜的质量为3.2g.
【点评】通过分析得出固体质量减少的质量即为参加反应氧化铜中氧元素质量,此为解答本问题的基础.

 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案下列各选项中,物质的分类均正确的是( )
| 选项 | 单质 | 氧化物 | 混合物 |
| A | 铝合金 | 氧化铜 | 稀盐酸 |
| B | 白磷 | 水 | 冰水混合物 |
| C | 氮气 | 干冰 | 空气 |
| D | 水银 | 硫酸钡 | 食盐水 |
A.A B.B C.C D.D
下列实验操作不能达到实验目的是
| 物 质 | 实验目的 | 实验操作 | |
| A | 硬水和软水 | 鉴 别 | 分别滴加肥皂水 |
| B | KNO3固体中混有少量NaCl | 分 离 | 溶解、过滤、蒸发、结晶 |
| C | Cu粉中含有少量Fe粉 | 除去Fe粉 | 加入硫酸铜溶液、再过滤、洗涤、干燥 |
| D | CaCl2和HCl混合溶液 | 除去 HCl | 加入过量CaCO3、过滤 |
( )
A.A B.B C.C D.D

 铁是生活中常用的金属。右图是某“取暖片”外包装的图片。该“取暖片”中发热剂主要成分有铁粉、活性炭、氯化钠、水等,其发热是利用铁生锈时会放热 。
铁是生活中常用的金属。右图是某“取暖片”外包装的图片。该“取暖片”中发热剂主要成分有铁粉、活性炭、氯化钠、水等,其发热是利用铁生锈时会放热 。