题目内容
9. 超市卖的纯碱产品中往往含有少量的氯化钠,化学兴趣小组的同学用某品牌的纯碱样品进行探究实验.他们取了5g该纯碱样品,在烧杯中配制成50g溶液,再向其中逐滴加入10%的氯化钙溶液,测得加入氯化钙溶液的质量与产生沉淀的质量关系如图所示.请回答下列问题:
超市卖的纯碱产品中往往含有少量的氯化钠,化学兴趣小组的同学用某品牌的纯碱样品进行探究实验.他们取了5g该纯碱样品,在烧杯中配制成50g溶液,再向其中逐滴加入10%的氯化钙溶液,测得加入氯化钙溶液的质量与产生沉淀的质量关系如图所示.请回答下列问题:(1)当加入氯化钙溶液40g时,烧杯中所得溶液的溶质是NaClNa2CO3.(写化学式)
(2)至恰好反应完全时,计算所得不饱和溶液的质量.(结果精确到0.1g)
分析 (1)根据图示分析,当加入氯化钙溶液40g时,碳酸钠没有被完全消耗解答;
(2)先根据化学方程式求出生成的沉淀的质量,再求出所得不饱和溶液的质量.
解答 解:
(1)由图示可知:当加入氯化钙溶液40g时,碳酸钠没有被完全消耗,碳酸钠和氯化钙反应生成氯化钠和碳酸钙沉淀,烧杯中所得溶液的溶质是NaCl Na2CO3;
(3)设生成沉淀的质量为x,参加反应的氯化钙的质量为:44.4g×10%=4.44g则
Na2CO3+CaCl2═CaCO3↓+2NaCl
111 100
4.44g x
$\frac{111}{4.44g}=\frac{100}{x}$
x=4g
所得不饱和溶液的质量=50g+44.4g-4g=90.4g
答案:(1)NaCl Na2CO3;
(2)所得不饱和溶液的质量是90.4g.
点评 该考点的命题方向主要是通过创设相关问题情景或图表信息等,来考查学生对根据化学反应方程式的计算步骤和格式的理解和掌握情况;以及阅读、分析、推断能力和对知识的迁移能力.并且,经常将其与“书写化学方程式、相对分子质量的计算、化学符号及其周围数字的意义、元素符号和化学式的意义、质量守恒定律及其应用、化学方程式的读法和含义、常见化学反应中的质量关系、溶液中溶质质量分数的有关计算、含杂质物质的化学反应的有关计算”等相关知识联系起来,进行综合考查.

练习册系列答案
相关题目
8.二氧化硅是玻璃的主要成分,二氧化硅(SiO2)中硅元素的化合价的是( )
| A. | +1 | B. | +2 | C. | +3 | D. | +4 |
9.铬和钼两种金属在现代科技发展中有着非常重要的作用,可用于电镀和制造特种钢,下列有关说法错误的是( )
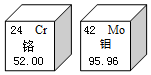

| A. | 在化学反应中,Cr原子和Mo原子都易失去电子 | |
| B. | 铬原子的质子数为24 | |
| C. | 铬原子的相对原子质量为52.00 | |
| D. | 钼离子的棱外电子数为42 |
4.下列实验操作正确的是( )
| A. |  点燃酒精灯 | B. |  检验氢气纯度 | ||
| C. |  称取一定质量的药品 | D. |  氧气验满 |
14.天平两边的托盘中分别装有等质量、等溶质质量分数的稀盐酸的烧杯,再将等质量的铝和铁分别加入两烧杯中,充分反应,下列说法正确的是( )
| A. | 若天平不平衡,则指针一定偏向铝的一侧 | |
| B. | 若天平不平衡,则两个烧杯中的酸一定有剩余 | |
| C. | 若反应后两烧杯中的金属均有剩余,则天平平衡 | |
| D. | 若反应后两烧杯中的酸均有剩余,则天平一定平衡 |
1.下列诗句描述的过程中包含化学变化的是( )
| A. | 千锤万凿出深山 | B. | 雪融山顶响流泉 | C. | 吹尽狂沙始到金 | D. | 蜡炬成灰泪始干 |
19.下列有关NaOH的描述中,正确的是( )
| A. | 用NaOH固体干燥CO2气体 | B. | 用酚酞溶液检验NaOH溶液是否变质 | ||
| C. | 用熟石灰和纯碱为原料制取NaOH | D. | 将NaOH固体放在纸张上进行称量 |