题目内容
15.如图是初中化学中常见物质间的转化关系,其中甲、乙、丙为单质;A、B、C、D、E为化合物;A在食品工业上是发酵粉的一种主要原料,D是使地球产生温室效应的一种气体,丙是目前世界上冶炼量最多的金属.(图中部分生成物已略去)
请回答下列问题:
(1)B中阴离子的化学符号是CO32-;E的名称为四氧化三铁;
(2)写出A受热分解的化学方程式2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑;
(3)在C生成甲和乙的化学反应中,所得甲、乙两种气体的体积比是1:2;(相同条件下)
(4)写出E与CO反应生成D和丙的化学方程式4CO+Fe3O4$\frac{\underline{\;\;△\;\;}}{\;}$3Fe+4CO2.
分析 本题属于推断题,根据题目给出的流程图和信息:A在食品工业上是发酵粉的一种主要原料,D是使地球产生温室效应的一种气体,丙是生产生活中占据主导地位的金属,因此A是碳酸氢钠,D是二氧化碳,丙是铁;碳酸氢钠在加热的条件下生成碳酸钠和水和二氧化碳,因此B是碳酸钠;水通电分解生成氢气和氧气,因此甲是氧气,乙是氢气,氧气和氢气的体积比是1:2;铁和氧气在点燃的条件下生成四氧化三铁,四氧化三铁和一氧化碳在高温的条件下生成铁和二氧化碳,配平即可.
解答 解:(1)碳酸氢钠在加热的条件下生成碳酸钠和水和二氧化碳,因此B是碳酸钠,碳酸钠中的阴离子是碳酸根离子;铁和氧气在点燃的条件下生成四氧化三铁,四氧化三铁和一氧化碳在高温的条件下生成铁和二氧化碳,故E为四氧化三铁;
(2)A在食品工业上是发酵粉的一种主要原料,因此A是碳酸氢钠,碳酸氢钠在加热的条件下生成碳酸钠和水和二氧化碳,配平即可;故答案为:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑;
(3)水通电分解生成氢气和氧气,又因为铁能在氧气中燃烧,因此甲是氧气,乙是氢气,氧气和氢气的体积比是1:2;
(4)四氧化三铁和一氧化碳在高温的条件下生成铁和二氧化碳,配平即可,故答案为:4CO+Fe3O4$\frac{\underline{\;高温\;}}{\;}$3Fe+4CO2.
故答案为:(1)CO32-;四氧化三铁;
(2)2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑;
(3)1:2;
(4)4CO+Fe3O4$\frac{\underline{\;\;△\;\;}}{\;}$3Fe+4CO2
点评 本考点属于图框式物质的推断题,是通过对实验方法和过程的探究,在比较鉴别的基础上,得出了正确的实验结论.本考点是中考的重要内容之一,是通过实验现象,从而得出物质的组成.书写化学方程式时,要注意配平,此考点主要出现在填空题和实验题中.

| A. |  闻气体的气味 | B. |  测溶液的pH值 | C. |  检查装置气密性 | D. |  酒精灯失火 |
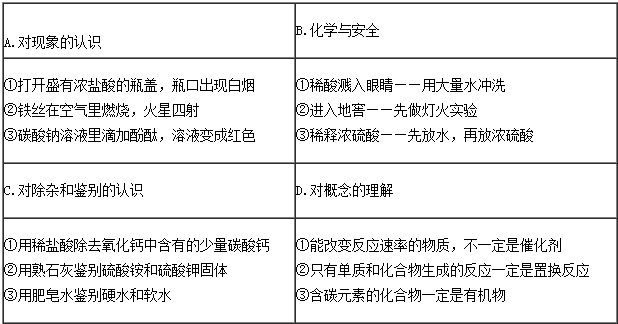
| A. | A | B. | B | C. | C | D. | D |
| A. |  熄灭酒精灯 | B. | 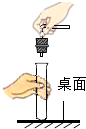 塞紧橡皮塞 | ||
| C. | 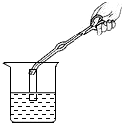 测定溶液的pH | D. | 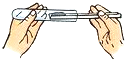 将固体粉末装入试管 |
| A. | 氧化物都是含氧元素的化合物 | B. | 分子是化学变化中的最小粒子 | ||
| C. | 有单质生成的反应都是置换反应 | D. | 电解水时负极产生的气体是氢气 |
| A. |  玻璃杯 | B. |  不锈钢杯 | C. |  塑料杯 | D. |  纸杯 |
| A. | 除去NaOH溶液中的Na2CO3,加入过量石灰水 | |
| B. | 鉴别稀盐酸和石灰水,分别滴加Na2CO3溶液 | |
| C. | 检验NaOH溶液是否显碱性,滴加酚酞溶液 | |
| D. | 分离CO和CO2,将混合气体通过足量NaOH溶液,再向所得溶液中加足量稀硫酸 |