题目内容
实验室用MnO2作为KClO3分解制取氧气的催化剂.杨洋查阅资料得知,CuO、Fe2O3等氧化物也能对KClO3分解起催化作用.杨洋想知道它们的催化能力是否相同,于是在实验室进行相关实验,获得数据如下:
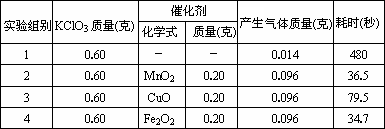
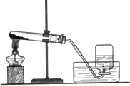
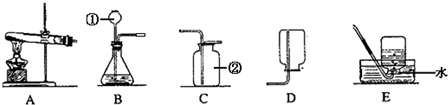
(1)已知KClO3、KCl溶于水,在催化剂回收过程中,要进行过滤操作,需要的玻璃仪器有玻璃棒、烧杯、________.
(2)本实验中,三种催化剂催化能力最弱的是________,此催化剂在此反应中的作用是________.
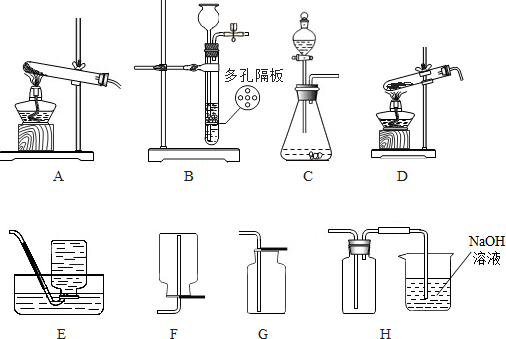
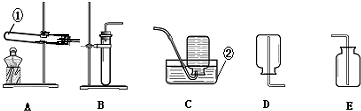
(3)停止加热时先把导管移出水面,其原因是________.
(4)将MnO2加入到8%的过氧化氢溶液里,产生的气体使带火星的木条________,为控制该反应的进行,请列举两个措施.
(5)利用表中数据,计算第2组实验中分解的KClO3的质量.
解析:
|
答案:(1) 漏斗 (2)CuO 加快反应速率 (3)防止水倒流回试管,导致试管破裂 (4)复燃 ①用分液漏斗控制滴加过氧化氢溶液的速率;②在布袋里装MnO2,用长线系好,控制布袋和过氧化氢溶液接触的速率 (5)0.245 g 讲析:(1)KClO3、KCl均溶于水,MnO2不溶于水,过滤分离不溶于水的固体混合物,需要用到玻璃棒、烧杯、漏斗三种玻璃仪器.(2)加入CuO作为催化剂的反应用时长,反应速率最慢.催化剂可以改变反应速率,不影响生成物的总质量,此反应中的催化剂起到加快反应速率的作用.(3)温度越高,气压越大,先撤酒精灯,温度会降低,压强减小,外界大气压迫使水槽中的水沿导管进入试管,会引起试管破裂.(4)固液试剂制取氧气,比较方便,只要能控制溶液和固体的接触速率,则可控制反应的进行. (5)答:(略). 解设:分解KClO3质量为x. 点评:此题是有关氧气的综合性试题.以开放性的实验探究形式考查有关催化剂、实验操作步骤、改进实验装置、利用化学方程式的简单计算等问题. |