题目内容
某地区的硫酸厂排出的尾气中含有SO2,废水中含有H2SO4,请回答:
(1)该地区经常下酸雨pH 5.6(填“<”、“>”或“=”).
(2)下列设施受酸雨的腐蚀作用最强的是 .
A.铜制塑像 B.大理石雕像 C.铝合金门窗 D.木制窗框
(3)用熟石灰处理该厂废水的化学方程式为 .
(1)该地区经常下酸雨pH
(2)下列设施受酸雨的腐蚀作用最强的是
A.铜制塑像 B.大理石雕像 C.铝合金门窗 D.木制窗框
(3)用熟石灰处理该厂废水的化学方程式为
考点:酸雨的产生、危害及防治,中和反应及其应用,书写化学方程式、文字表达式、电离方程式
专题:化学与环境保护
分析:(1)根据酸雨的PH范围和酸雨的性质进行分析、判断,从而得出正确的结论;
(2)根据质量守恒定律可以书写化学方程式;
(3)化石燃料燃烧时能产生大量的二氧化硫、二氧化氮等物质,这些物质能和水反应生成显酸性的物质,当酸性达到一定程度时会形成酸雨,结合酸的性质来回答.
(2)根据质量守恒定律可以书写化学方程式;
(3)化石燃料燃烧时能产生大量的二氧化硫、二氧化氮等物质,这些物质能和水反应生成显酸性的物质,当酸性达到一定程度时会形成酸雨,结合酸的性质来回答.
解答:解:
(1)当雨水的PH小于5.6时称为酸雨.
(2)
A、酸雨显酸性,铜的化学性质不活泼,不能和酸雨中的物质反应,故错误;
B、大理石中的碳酸钙能和显酸性的物质剧烈反应,腐蚀比较明显,故正确;
C、铝制窗框含有的金属铝能与酸反应,但铝表面的氧化膜的保护作用,故腐蚀较轻,故错误;
D、木制窗框不能与酸雨中的酸性物质反应,故错误.
(3)氢氧化钙和硫酸反应生成硫酸钙和水,反应的化学方程式为:Ca(OH)2+H2SO4═CaSO4+2H2O;故填:Ca(OH)2+H2SO4═CaSO4+2H2O.
答案:
(1)<
(2)B
(3)Ca(OH)2+H2SO4═CaSO4+2H2O
(1)当雨水的PH小于5.6时称为酸雨.
(2)
A、酸雨显酸性,铜的化学性质不活泼,不能和酸雨中的物质反应,故错误;
B、大理石中的碳酸钙能和显酸性的物质剧烈反应,腐蚀比较明显,故正确;
C、铝制窗框含有的金属铝能与酸反应,但铝表面的氧化膜的保护作用,故腐蚀较轻,故错误;
D、木制窗框不能与酸雨中的酸性物质反应,故错误.
(3)氢氧化钙和硫酸反应生成硫酸钙和水,反应的化学方程式为:Ca(OH)2+H2SO4═CaSO4+2H2O;故填:Ca(OH)2+H2SO4═CaSO4+2H2O.
答案:
(1)<
(2)B
(3)Ca(OH)2+H2SO4═CaSO4+2H2O
点评:本题主要考查了化学方程式的书写、节能环保理念的培养及其酸雨的形成与危害等方面的内容.

练习册系列答案
 新课标同步训练系列答案
新课标同步训练系列答案
相关题目
“金秋送爽,丹桂飘香”,金秋季节,你漫步在温馨的校园里能闻到沁人心扉的桂花香味,这是因为( )
| A、分子的体积很小 |
| B、分子在化学变化中可分 |
| C、分子之间有间隔 |
| D、分子总是不停地运动 |

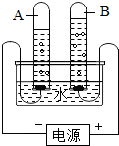 (1)如图是电解水的实验装置图.电解水的化学方程式为
(1)如图是电解水的实验装置图.电解水的化学方程式为